Neurotransmitter, die von Nervenenden freigesetzt werden, binden an spezifische Rezeptoren, bei denen es sich um spezialisierte Makromoleküle handelt, die in die Zellmembran eingebettet sind. Die Bindungswirkung löst eine Reihe spezifischer biochemischer Reaktionen in der Zielzelle aus, die eine physiologische Reaktion hervorrufen. Diese Effekte können durch verschiedene Medikamente, die als Agonisten oder Antagonisten wirken, modifiziert werden.,
Das autonome System besteht aus zwei Hauptabteilungen: dem sympathischen Nervensystem und dem parasympathischen Nervensystem. Diese funktionieren oft antagonistisch. Ein Signal wird vom Rückenmark durch zwei aufeinanderfolgende Neuronen in periphere Bereiche übertragen. Das erste Neuron (präganglionär), das aus dem Rückenmark stammt, synapsiert mit dem zweiten Neuron (postganglionär) in einem Ganglion. Parasympathische Ganglien neigen dazu, nahe oder innerhalb der Organe oder Gewebe zu liegen, die ihre Neuronen innervieren, während sympathische Ganglien an einer weiter entfernten Stelle von ihren Zielorganen liegen., Beide Systeme haben assoziierte sensorische Fasern, die Rückkopplungsinformationen in das zentrale Nervensystem bezüglich des funktionellen Zustands von Zielgeweben senden.
Der signifikante Unterschied zwischen den beiden Systemen besteht darin, dass ihre postganglionären Fasern verschiedene Neurotransmitter absondern. Diejenigen des parasympathischen Systems sezernieren Acetylcholin (ACh), daher der Name cholinergisch, während die postganglionären Fasern Noradrenalin (NE) absondern, daher der Name adrenergisch. Die präganglionischen Fasern beider Systeme sezernieren ACh; Daher sind beide präganglionischen Fasern cholinerg., Motoneuronen, die nicht Teil des autonomen Nervensystems sind, setzen auch Acetylcholin frei (siehe Abbildung 1).
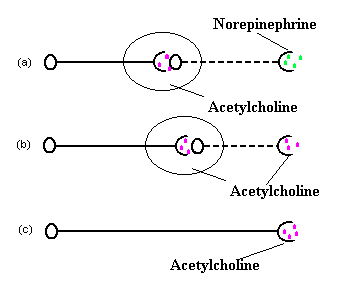
Abbildung 1. (a) Präganglionische Neuronen (durchgezogene Linie) der sympathitischen Teilung des autonomen Nervensystems setzen Acetycholin an ihren Synapsen mit postganglionischen Neuronen frei (gestrichelte Linie). Obwohl Ausnahmen auftreten, setzen die postganglionären Neuronen bei ihrer Funktion mit Effektoren hauptsächlich Noradrenalin frei., (b) Prägangionische Neuronen (durchgezogene Linie) der parasympathischen Teilung des autonomen Nervensystems setzen Acetycholin an ihren Synapsen mit postganglionischen Neuronen (gestrichelte Linie) frei, und die postgangionischen Neuronen setzen auch Acetycholin an ihren Effektoren frei. (c) Somatische efferente Neuronen setzen Acetylcholin an ihren Verbindungsstellen mit Skelettmuskeln frei.S. K. Anderson
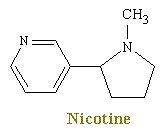
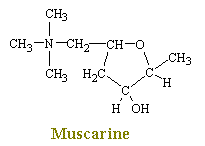
Acetylcholin wirkt auf mehr als einen Rezeptortyp., Henry Dale, ein britischer Physiologe, der 1914 in London arbeitete, stellte fest, dass zwei Fremdstoffe, Nikotin und Muskarin, jeweils einige, aber nicht alle der parasympathischen Wirkungen von Acetylcholin nachahmen konnten. Es wurde gefunden, dass Nikotin Rezeptoren auf Skelettmuskulatur und sympathischen und parasympathischen postganglionären Neuronen stimuliert, jedoch stimuliert Muscarin Rezeptorstellen nur an der Kreuzung zwischen postganglionären parasympathischen Neuronen und dem Zielorgan. Dale klassifizierte daher die vielen Wirkungen von Acetylcholin in nikotinische und muskarinische Wirkungen., Es ist anschließend klar geworden, dass es zwei verschiedene Arten von Acetylcholinrezeptoren gibt, die entweder von Muscarin oder Nikotin betroffen sind. Um dies erneut zu bekräftigen, verursachen Nikotinrezeptoren, dass sympathische postganglionische Neuronen und parasympathische postganglionische Neuronen feuern und ihre Chemikalien und Skelettmuskeln freisetzen, um sich zusammenzuziehen. Muskarinrezeptoren sind hauptsächlich mit parasympathischen Funktionen assoziiert und stimulieren Rezeptoren in peripheren Geweben (z. B. Drüsen, glatte Muskulatur). Acetylcholin aktiviert alle diese Stellen.,
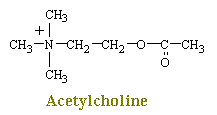
Fortgeschrittene biochemische Techniken haben nun einen grundlegenderen Unterschied in den beiden Arten cholinerger Rezeptoren gezeigt. Der Nikotinrezeptor ist ein Kanalprotein, das sich bei Bindung durch Acetylcholin öffnet, um die Diffusion von Kationen zu ermöglichen. Der Muskarinrezeptor hingegen ist ein Membranprotein; Bei Stimulation durch Neurotransmitter bewirkt er indirekt die Öffnung von Ionenkanälen durch einen zweiten Boten. Aus diesem Grund ist die Wirkung einer muskarinischen Synapse relativ langsam., Muskarinrezeptoren überwiegen auf höheren Ebenen des Zentralnervensystems, während Nikotinrezeptoren, die viel schneller wirken, bei Neuronen des Rückenmarks und an neuromuskulären Übergängen im Skelettmuskel häufiger vorkommen.
Ein Cholinergikum ist eines von verschiedenen Arzneimitteln, die die Wirkung des Neurotransmitters Acetylcholin im Körper hemmen, verstärken oder nachahmen. Acetylcholinstimulation des parasympathischen Nervensystems hilft, glatte Muskeln zusammenzuziehen, Blutgefäße zu erweitern, Sekrete zu erhöhen und die Herzfrequenz zu verlangsamen., Einige cholinerge Medikamente wie Muscarin, Pilocarpin und Arecolin ahmen die Aktivität von Acetylcholin bei der Stimulierung des parasympathischen Nervensystems nach. Diese Medikamente haben jedoch nur wenige therapeutische Anwendungen. Andere cholinerge Medikamente wie Atropin und Scopolamin hemmen die Wirkung von Acetylcholin und unterdrücken so alle Wirkungen des parasympathischen Nervensystems. Diese Medikamente helfen, solche Körpersekrete wie Speichel und Schleim auszutrocknen und glatte Muskelwände zu entspannen., Sie werden therapeutisch eingesetzt, um Krämpfe der glatten Muskelwände des Darms zu lindern, Bronchialkrämpfe zu lindern, Speichelfluss und Bronchialsekrete während der Anästhesie zu verringern und die Pupille während ophthalmologischer Eingriffe zu erweitern.
Nikotin
Nikotin ist eine organische Verbindung, die das Hauptalkaloid von Tabak ist. Nikotin kommt in der gesamten Tabakpflanze und insbesondere in den Blättern vor. Die Verbindung macht etwa 5 Prozent der Pflanze nach Gewicht aus., Sowohl die Tabakpflanze (Nicotiana tabacum) als auch die Verbindung sind nach Jean Nicot benannt, einem französischen Botschafter in Portugal, der 1550 Tabaksamen nach Paris schickte.
Rohes Nikotin war 1571 bekannt, und die Verbindung wurde 1828 in gereinigter Form erhalten; Die richtige molekulare Formel wurde 1843 festgelegt, und die erste Laborsynthese wurde 1904 berichtet. Nikotin ist eines der wenigen flüssigen Alkaloide. In seinem reinen Zustand ist es eine farblose, flüchtige Basis (pKa).,5) mit einer öligen Konsistenz, aber wenn es Licht oder Luft ausgesetzt wird, erhält es eine braune Farbe und gibt einen starken Tabakgeruch ab.

Die komplexen und oft unvorhersehbaren Veränderungen, die im Körper nach der Verabreichung von Nikotin auftreten, sind nicht nur auf seine Wirkungen auf eine Vielzahl von Neuroeffektoren und chemosensitiven Stellen zurückzuführen, sondern auch auf die Tatsache, dass das Alkaloid sowohl stimulierende als auch depressive Wirkphasen aufweist. Die ultimative Reaktion eines Systems stellt die Summe der verschiedenen und entgegengesetzten Wirkungen von Nikotin dar., Zum Beispiel kann das Medikament die Herzfrequenz durch Anregung von sympathischen Herzganglien erhöhen, und es kann die Herzfrequenz durch Stimulation von parasympathischen Herzganglien verlangsamen. Darüber hinaus beeinflussen die Wirkungen des Arzneimittels auf die Chemorezeptoren des Carotis-und Aortenkörpers sowie auf die Markzentren die Herzfrequenz sowie die kardiovaskulären Kompensationsreflexe, die sich aus durch Nikotin verursachten Blutdruckänderungen ergeben. Schließlich verursacht Nikotin einen Ausfluss von Adrenalin aus dem Nebennierenmark, und dieses Hormon beschleunigt die Herzfrequenz und erhöht den Blutdruck.,
Nikotin ist einzigartig in seiner zweiphasigen Wirkung. In der Medulla rufen kleine Dosen Nikotin den Ausfluss von Katacholaminen hervor und verhindern in größeren Dosen deren Freisetzung als Reaktion auf die Nervenstimulation. Seine zweiphasige Wirkung bewirkt eine stimulierende Wirkung, wenn sie in kurzen Zügen eingeatmet wird, aber wenn sie in tiefen Zügen geraucht wird, kann sie beruhigend wirken. Aus diesem Grund kann sich das Rauchen manchmal belebend anfühlen und stressige Reize bei anderen blockieren.
Nikotin stimuliert deutlich das zentrale Nervensystem (ZNS)., Geeignete Dosen erzeugen Zittern sowohl bei Menschen als auch bei Labortieren; Bei etwas größerer Dosis folgen dem Zittern Krämpfe. Die Erregung der Atmung ist eine prominente Wirkung von Nikotin; Obwohl große Dosen direkt auf die Medulla oblongata wirken, verstärken kleinere Dosen die Atmung reflexartig durch Erregung der Chemorezeptoren der Carotis und der Aortenkörper. Auf die Stimulation der CNA folgt eine Depression, und der Tod resultiert normalerweise aus einem Versagen der Atmung aufgrund der zentralen Analyse und der peripheren Blockade der Atemmuskulatur., Nikotin verursacht auch Erbrechen durch zentrale und periphere Handlungen. Die zentrale Komponente der Brechreaktion ist auf die Stimulation der Chemorezeptor-Triggerzone in der Medulla zurückzuführen.oblongata. Darüber hinaus aktiviert Nikotin vagale und spinale afferente Nerven, die vom sensorischen Eingang der Reflexwege, die am Erbrechen beteiligt sind.
Obwohl Acetylcholin eine Vasodilatation und eine Abnahme der Herzfrequenz verursacht, führt Nikotin bei intravenöser Verabreichung an den Hund charakteristisch zu einem Anstieg der Herzfrequenz und des Blutdrucks., Dies liegt daran, dass die kardiovaskulären Reaktionen auf Nikotin im Allgemeinen auf die Stimulation der sympathischen Ganglien und des Nebennierenmarks zusammen mit der Abgabe von Katacholaminen aus sympathischen Nervenenden zurückzuführen sind.
Nikotin wird kommerziell aus Tabakresten gewonnen und wird als Insektizid und als Tierarzneimittel (Wurmer) verwendet. Salpetersäure oder andere Oxidationsmittel wandeln Nikotin in Nikotinsäure oder Niacin um, das als Nahrungsergänzungsmittel verwendet wird.,=“e3a86e869c“>
Nicotine Addiction
| Link 1 | |
| Link 2* |
Miscellaneous
| How deadly is nicotine?, (don ‚ T nehmen diese Webseite zu ernst) | |
| Nikotin-Dosierungen |
Muscarin
Muscarin, und alkaloid, erhalten von den giftigen Pilz Amanita Muscaria, produziert die Effekte vorhersagbar von der stimulation der postgangiolinc parasympathische Fasern. Die Symptome treten normalerweise innerhalb von 15-30 Minuten nach Einnahme oder Injektion auf und konzentrieren sich auf das unwillkürliche Nervensystem., Die Muskarinalkaloide stimulieren die glatte Muskulatur und erhöhen dadurch die Beweglichkeit; große Dosen verursachen Krämpfe und schweren Durchfall. Die Bronchialmuskulatur wird ebenfalls stimuliert und verursacht asmatische Anfälle. Übermäßiger Speichelfluss, Schwitzen, Tränen, Stillzeit (bei schwangeren Frauen) sowie starkes Erbrechen treten ebenfalls auf. Die auffälligsten kardiovaskulären Effekte sind ein deutlicher Blutdruckabfall und eine Verlangsamung oder vorübergehende Beendigung des Herzens. Opfer erholen sich normalerweise innerhalb von 24 Stunden, aber schwere Fälle können zum Tod aufgrund von Atemversagen führen., Alle Wirkungen von muskarinähnlichen Arzneimitteln werden durch das Alkaloid Atropin verhindert. Darüber hinaus zeigen weder atropinähnliche noch muskarinähnliche Medikamente Wirkungen am neuromuskulären Übergang.

Obwohl Muscarine und Muscarine wie Alkaloide von großem Wert als pharmakologische Werkzeuge sind, ist die gegenwärtige klinische Verwendung weitgehend eingeschränkt. Seit sich Hinweise häufen, dass es unterschiedliche Subtypen von Muskarinrezeptoren gibt, besteht ein erneutes Interesse an synthetischen Analoga, die die Gewebeselektivität von muskarinischen Agonisten verbessern können.,
Mitwirkende und Aufgaben
-
Edward B. Walker (Weber State University)