Úvod
porozumění a řízení V/Q vztahů představuje acornerstone z jednotky intenzivní péče (JIP) pacienta. Vztah TheV / Q (obr. 1) lze považovat za spektrum meziprostor (nekonečný v/Q) a zkrat (nula V/Q).
Když pulmonarycapillary krev je vystavena alveolární parciální tlak ofoxygen (PAO2), molekuly kyslíku přesunout do theplasma jako rozpuštěný O2 a nadále vyvíjet partialpressure.,
Většina těchto molekul kyslíku okamžitě spojit withhemoglobin a vstoupit do stavu, ve kterém již přímo exerta parciální tlak. Tento proces pokračuje, dokud částečné pressuregradient mezi alveolus a plazmové již neexistuje, o níž bod hemoglobin je maximálně nasycen pro bloodPO2.
I když kyslík rozpuštěný v plasmarepresents pouze 1,5 % až 3 % celkového kyslíku v krvi, thePO2 hodnoty je důležité, protože to určuje drivingforce pro kyslík pohyb do a z krve.,
Ideální bloodgas výměna by vyžadovalo každý alveolus být ventilatedperfectly a všechna krev vysune z pravé komory totraverse zcela funkční plicní kapiláry. Navíc by musela být provedena difúze přes alveolární / kapilární membránu.
Protože všechna krev prochází z pravé komory do levé komory by se dosáhnout dokonalé rovnováhy s alveolargas, alveolární PO2 (PAO2) a arteriální PO2 (PaO2) by beidentical.
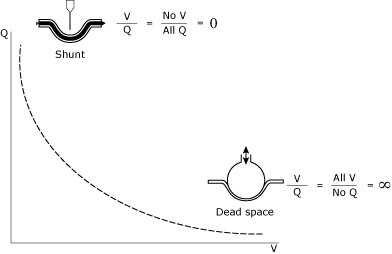
obr. 1., Matematická a konceptuální ilustrace zkratu a deadspace.
, jak je znázorněno na obr. 2, okysličení v normálních plicích můželiší se od ideální situace, protože distribuce perfusionis nerovnoměrné.
Relativně větší průtok krve se vyskytuje v thegravity oblasti závislé, a některé žilní drenáž (z thebronchial, pleurální a Thebesian žíly) se vlévá přímo do levý straně srdce, a tak obcházet (posunovací) normaloxygenation mechanismus .,
z tohoto Důvodu, krev vstupuje levý komory s nižším obsahu kyslíku než bloodexchanging s ideální alveolus. Obrázek 3 představuje nižší úroveň PaO2 ve srovnání s vypočteným ideálním napětím kyslíku.
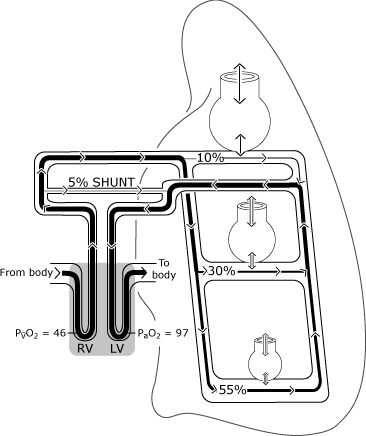
obr. 2. Normální plíce mají nedokonalé rozložení ventilace a perfuze, která je primárně určena gravitací. Obrázek předpokládá vzpřímené držení těla tak, aby plicní základny byly v gravitačně závislé poloze., Alveoly závislé na gravitaci jsou větší, ale dostávají méně výměny plynu (větrání) než alveoly závislé na gravitaci. Distribuce perfúze je primárně řízena gravitací, přičemž přibližně 55 % proudí do oblastí závislých na gravitaci, 30% do oblastí středních plic a 10% do oblastí plic závislých na gravitaci. PaO2 a PvO2 jsou vyjádřeny v mmHg (kPa = mmHg × 0,133); RV = pravá komora; LV = levá komora. Reprodukováno se souhlasem Elsevier Health Sciences.
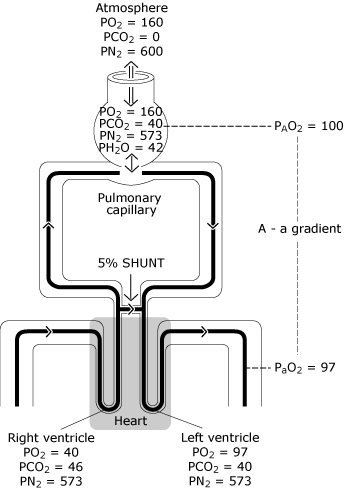
obr. 3., Normální plíce mají nedokonalé rozložení ventilace, nedokonalé rozdělení perfúze a minimální stupeň intrapulmonálního posunu. Výsledkem je pokles PO2 z vypočtené ideální alveolární hodnoty (PAO2) na měřenou systémovou arteriální krevní hodnotu (PaO2). Tento rozdíl PO2 je známý jako „gradient napětí alveolárního až arteriálního kyslíku“. PO2 = napětí kyslíku vyjádřené v mmHg; PCO2 = napětí oxidu uhličitého vyjádřené v mmHg; PN2 = napětí dusíku vyjádřené v mmHg; PH2O = napětí vodní páry vyjádřené v mmHg. (kPa = mmHg × 0.133)., Reprodukováno se souhlasem Elsevier Health Sciences.
Zkrat a hypoxémie
Anatomické posun je definován jako krev, která jde z pravé sideto levé straně srdce bez pojezdu plicní kapiláry. Kapilární posun je definován jako krev, která jde z pravé strany srdce na levé straně srdce viapulmonary kapilár, které jsou přilehlé k neventilovaných alveolů.
oba případy umožňují vstup krve do levostranného oběhu bezzvýšení obsahu kyslíku., Toto je označováno jako nula V / Q, nebotrue posun, protože krev neměla příležitost pro výměnu plynů s funkčními alveoly.
příkladem posunu vklinickém prostředí jsou abnormality výměny plynu pozorované vpneumonii uvolněním endotoxinu, které vede k buněčnému edémua vazokonstrikci .
posun a hypoxemie nejsou synonymní pojmy, ani jejichmají lineární vztahy. Na hypoxémií účinek derivační willdepend nejen na velikosti zkratu, ale také na oxygenationstatus žilní krev, která bočníky(SVO2)., Malý zkrat s lowSVO2 může mít hluboké hypoxemické účinky, zatímco velký zkrat s vysokým SvO2 budepříčinou méně významné hypoxémie.
To může být uvedeno jednoznačně, že když hypoxémie existuje, somedegree posunovacích (intrapulmonární nebo intrakardiální) musí bepresent; nicméně, účinek zkrat na thePaO2 značně závisí na cardiovascularfunction a metabolismus. Arteriální hypoxemie je důsledkem plicefunkce, kardiovaskulární funkce a metabolismus.,
hodnocení lungs jako oxygenátor je nezbytný v péči mnoha pacientůvyžadující kardiopulmonální podpůrnou péči. Výpočet intrapulmonálního posunu představuje nejlepší dostupné prostředkyodstranit, do jaké míry přispívá plicní systémhypoxemie.
Intrapulmonární zkratu
Jak bylo uvedeno dříve, intrapulmonární bočníku je definovaná jako thatportion z arteriálního vstupu na levé straně heartwithout prochází perfektní výměna plynů s úplně functionalalveoli. Intrapulmonální zkrat lze rozdělit na třikomponenty.,
- anatomický posun byl dříve popsán jako krev, která vstupuje do levé strany srdce, aniž by procházela plicními kapilárami. Kromě normálních anatomických posun z průdušek, pohrudnice a Thebesian žíly, anatomické posunování může být zvýšena tím, cévní nádory plic a pravý-k-levé intrakardiálních zkratů.
- Kapilární posun je způsobena, když krev prochází plicními kapilárami, ale není srovnat s alveolárním plynu v důsledku patologických procesů, např. atelektázy, pneumonie a akutní poranění plic.,
- žilní příměs nastává, když se krev vyrovnává s alveolárním PO2, který je méně než ideální jako v situacích s nízkým V / Q . Protože žilní příměs není pravda, zkrat, to někdy vede ke zmatku. Součet anatomických a kapilárních zkratů se nejčastěji nazývá nulový v / Q nebo pravý zkrat. Žilní příměs je často označována jako nízký v / Q nebo „shunt effect“. Fyziologický zkrat v normálních nebo ne-nemocných plicích je měření normálního intrapulmonálního zkratu. Při stanovení plicní patologie představuje fyziologický zkrat především závažnost onemocnění.,
derivační rovnice
rovnice použité pro výpočet derivační část z srdeční výdej předpokládá, že non-posunovací plynu perfectlyoxygenates výměnou s perfektní alveolární plyn.
ačkoli koncept intrapulmonálního zkratu neodráží regionálnírelationships, stejně jako koncept perfúze ventilace, neodráží stupeň, do kterého se plíce odchylují od ideálu jako anoxygenátor plicní krve.
je To právě tato kvantitativní schopnost vypadat na plíce jako oxygenátorem, že je to measurementunique a cenné v klinickém prostředí., Tento přehled používá thetem fyziologický zkrat s odkazem na intrapulmonální shuntcalculated s dýcháním pacienta méně než 100% kyslíku.
odvození rovnice zkratu pochází z pojmů ofFick. V roce 1870 byl zaveden klasický vztah, který thequantity kyslíku k dispozici pro využití tkáně za jednotku timeincludes arteriální obsah kyslíku (CaO2)vynásobí množství arteriální krve prezentovány thetissues za jednotku času (tj., srdeční výdej, Qt).,
Rovnice 1:
Kyslík k dispozici =(Qt)(CaO2)
Kyslík se vrátil do plic, obsahuje srdeční výdej(Qt) vynásobí smíšené žilní obsah kyslíku(CVO2).
Rovnice 2,
Kyslík se vrátil =(Qt)(CvO2)
spotřeba Kyslíku za jednotku času (VO2) by reflectthe kyslíku, které byly extrahovány z krve v timeperiod.,
Rovnice 3:
VO2 = (Qt)(CaO2)– (Qt)(CvO2)
Rovnice 3, pak může být přepsána jako to, co je classicallydescribed jako Fick Rovnice.
Rovnice 4:
VO2 = Qt(CaO2 –CvO2)
Předělaný algebraicky, Rovnice 4 může být vyjádřen jako funkce srdečního výdeje.,
Rovnice 5:
Qt = VO2/(CaO2 –CvO2)(10)
vyjádřit srdeční minutový objem v litrech za minutu, oxygendifference musí být
násobí koeficientem 10.
další Dvě rovnice, s níž se musí seznámit se vymyká klasickému derivační rovnice (Rovnice 6), který popisuje ratiobetween odsunut srdeční výdej a celkový srdeční výdej(QS/Qt). Měří se u pacientadýchání 100% kyslíku.,
Rovnice 6:
QS/Qt = (CcO2 –CaO2)/(CcO2 –CvO2)
fyziologický shunt rovnice (QSP/Qt) isanother způsob, jak vyjádřit Rovnice 6 při měření s patientbreathing méně než 100 % kyslíku a některé žilní příměs existuje.Proto fyziologický shunt rovnice je:
Rovnice 7:
QSP/Qt = (CcO2 –CaO2)/ (CcO2 –CvO2)
QSP/Qt má tu výhodu, že beingderived jako poměr tak, že žádná absolutní měření srdečního výdeje isrequired., V této podobě, rovnice jasně ukazuje, že jak odsunut srdeční výdej přístupy nula, arteriální oxygencontent musí blížit teoretické end plicní capillaryoxygen obsahu.
tak dlouho, Jak některé části srdeční výdej doesnot dokonale exchange s perfektní sklípků, arteriální oxygencontent musí být méně než ideální konci plicní kapiláry oxygencontent.
důsledky fyziologického shunt rovnice může býtkonceptualizován s ohledem na obsah kyslíku termíny (CcO2, CaO2, CvO2)jako entity, které mohou být nalita do acontainer (obr. 4)., Některé faktory, jako je hemoglobinkoncentrace, mohou ovlivnit všechny tři úrovně.
nejdůležitějšíklinická proměnná ovlivňující CcO2 isFiO2, zatímco celkový srdeční výkon i spotřeba kyslíku ovlivňují CvO2. Změny ve fyziologickém zkratu ovlivňují CaO2.
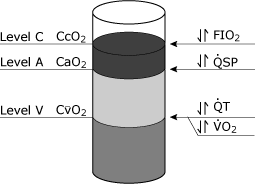
obr. 4. Schematické znázornění hladin kyslíku v krvi, které by mohly být teoreticky získány ze tří samostatných míst v kardiovaskulárním systému. Úroveň C představuje konec plicní kapilární obsah kyslíku v krvi (CcO2)., Úroveň a představuje systémový obsah arteriálního kyslíku v krvi (CaO2) a hladina v představuje smíšený obsah žilního (plicní tepny) kyslíku v krvi (CvO2). Nejčastější klinické proměnné, které se konkrétně dotýkají tyto různé úrovně je uvedeno: Úroveň C je nejčastěji ovlivněna změnami v FIO2 (frakce vdechovaného kyslíku), Úroveň je specificky ovlivněn změnami ve fyziologické zkratu (QSP), Stupeň V je specificky ovlivněna jak celkový srdeční výdej (QT) a rychlost spotřeby kyslíku (VO2). Reprodukováno se souhlasem Elsevier Health Sciences.,
čitatel rovnice zkratu je reprezentovánrozdíly v CcO2 acao2. Jmenovatel rovnice jepředstavené rozdíly v CcO2 acvo2.
změny nerovnoměrné velikosti mezityto tři úrovně změní poměr, což je ekvivalentzměny ve fyziologickém výpočtu zkratu.
Pokud pacient developsfulminant pravé, střední a dolní lalok konsolidace, thearterial a plicní tepny krevní plyny měření odhalí aclinical obrázek, jak se odráží v Obr. 5.,
arteriální oxygentenze a obsah jsou významně sníženy kvůli velkémuintrapulmonální zkrat. Pokud je srdeční výdej zůstává beze změny a arteriální-smíšené žilní kyslíku rozdíl nemění, potom CvO2 musí také snížit.
Kvůlirozsah nerovného rozsahu, fyziologický zkrat bude velkýzvýšit sekundární hypoxemii.
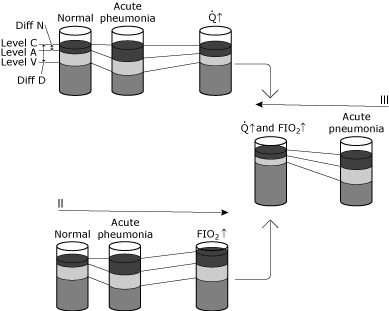
obr. 5. Schematické znázornění změn hladin kyslíku v krvi za různých podmínek., Účelem této ilustrace je konceptualizovat rozdíl mezi fyziologickým posunem a hypoxemickým účinkem fyziologického posunu. I, II, a III ilustrují změny v normální jedince, kteří smlouvy pneumonitida, která způsobuje výrazné zvýšení intrapulmonární posunování bez jakýchkoliv kompenzačních fyziologické změny., Stav od normální k akutní pneumonii ukazuje: žádná změna úrovně C, protože ventilace a FIO2 se nemění, specifický pokles hladiny A v důsledku zvýšeného posunu vytvořeného pneumonií a pokles hladiny v, protože rozdíl obsahu AV se nemění (srdeční výdej a spotřeba kyslíku beze změny). Vzhledem k tomu, že Diff N se zvýšil ve větší míře než Diff D, vypočítaný zkrat se zvyšuje. Stav 1 ukazuje zvýšený srdeční výdej (Q↑) v reakci na akutní hypoxemii. Úroveň C zůstává nezměněna, protože nebyla změněna ventilace ani FIO2., Rozdíl v obsahu AV se zúžil, protože srdeční výdej se zvýšil, zatímco spotřeba kyslíku zůstává nezměněna. Zvýšení úrovně V vede k nové dynamické rovnováze, ve které se také zvyšuje úroveň a. Všimněte si, že vztah mezi Diff N A Diff D je jen mírně změněn. Úroveň A (a tedy PaO2) se tak zvýšila s malou změnou vypočteného zkratu. V tomto případě je kompenzace hypoxémie kardiovaskulární; intrapulmonální zkrat se nezměnil. Stav II vykazuje zvýšenou inspirovanou koncentraci kyslíku (FIO2↑)., Úroveň C se zvyšuje, zatímco rozdíl obsahu AV zůstává nezměněn(srdeční výdej a spotřeba kyslíku beze změny). Nová dynamická rovnováha má za následek úroveň a (a tedy zvýšení PaO2). Vztah mezi Diff N A Diff D je jen mírně změněn. Úroveň a (a tedy PaO2) se zvýšila s malou změnou vypočteného zkratu. V tomto případě je kompenzace hypoxémie prostřednictvím kyslíkové terapie; intrapulmonální zkrat je v podstatě nezměněn. Stav III ukazuje jak srdeční výdej, tak inspirované změny koncentrace kyslíku (Q↑ A FIO2↑)., Všimněte si hlubokého zvýšení úrovně A (a tedy PaO2) s malou změnou v Diff N/Diff D.reprodukované se souhlasem Elsevier Health Sciences.
těžká hypoxemie obvykle povede ke zvýšení kardiovýstupu. To má za následek snížení arteriálně-žilního oxygencontentního rozdílu, který se odráží zvýšením inCvO2.
nová rovnováha povede ke zvýšení CaO2 bez změny poměru (QSP / Qt). Arteriální Po2zlepšuje výrazně, bez významné změny fyziologických zkratůsekundární, kvůli zlepšenému srdečnímu výkonu.,
Pokud se předpokládá, že doplňkový kyslík je podáván tomuto pacientovi, zatímco srdeční výdej zůstávánezměněn, CcO2 se zvyšuje sekundárně na aninkurovanou alveolární PO2. Vzhledem k fyziologické shuntremains stejné a arteriální-venózní obsah kyslíku differenceremains stejné, nové rovnováhy výsledky inCaO2 a CvO2increasing.
nakonec se okolnosti změní tak, aby zobrazovaly pacienta soxygenovou terapií a zvýšením srdečního výdeje.CaO2 se zvyšuje, protože bothcco2 a CvO2 se zvyšují.Hypoxemie se zlepšuje, zatímco poměr (QSP / QT) zůstává nezměněn.,
fyziologický výpočet zkratu může spolehlivě odrážetstupeň výměny plynu připadající na intrapulmonární onemocnění nebointrakardiální posun bez ohledu na další faktory, které mohou takéhraje roli.
Protože více příčiny hypoxemie jsou frequentlyencountered u kriticky nemocných, schopnost kvantifikovat thedegree z intrapulmonární patofyziologie je velmi importanttool.
jak zjistit zkrat
intrapulmonální zkrat lze měřit pouze tehdy, když jsou k dispozici arteriální a plicní arteriální krevní vzorky a FIO2 je konstantní., Katetry insertedinto centrální žilní oběh, který leží těsně nad thesuperior duté žíly-pravé síně křižovatky jsou do značné míry nedostatečné forshunt stanovení, protože krev z této pozice nebude obsahovat výrazně desaturated krev z coronarysinus nebo dolní duté žíly.
vzorky krve odebrané z rightatria vykazují významnou změnu obsahu kyslíku kvůlikaneling průtoku krve a pohyb špičky katétru. Katetripy v pravé komoře mohou způsobit ventrikulární ektopii a výtěžekvariabilní vzorky obsahu kyslíku., Jsou získány smíšené žilní vzorkyz katétru plicní tepny.
normální hodnoty jsou střední částečnétlak O2 ve smíšené žilní krvi 40 mmHg (SVO2 75 %).
Pokud je to vůbec možné, pacient by neměl být stimulován nebo několik minut před odběrem vzorků. Je třeba dbát na to, aby se během této doby zabránilo sání dýchacích cest a dalším postupům. Arteriální a smíšený žilní vzorek by měl být nakreslensoučasně. Je třeba dbát na to, aby nedošlo k chybám při odběru vzorků, zejména z katétru plicní arterie.,
Když krev samplesare čerpány z plicní tepny, musí být vzorek drawnslowly, protože rychlé vdechnutí může způsobit plicní capillaryblood být smíchán s plicní tepny krev, což způsobuje dramaticincreases v obsahu kyslíku .
Rychlý tok intravenózní fluidsvia centrálního žilního katétru nebo více proximální PA katetru scannování kontaminovat krev z distální port PA catheterand způsobit chybné stanovení hemoglobinu a kyslíku contentcalculations.
vypočítají se hodnoty CaO2 a Cvo2., Mezi obsahem hemoglobinu obou vzorků by nemělo být více než 1 g/dlrozdíl. Průměrný dvou se doporučuje pro výpočty, pokud si rozdílu je větší než 0,5 g/dL.
doporučuje se změřit nebo předpokládat 1, 5% karboxyhemoglobinu . TheCcO2 hodnota je pak vypočtena pomocí průměrnou nebo arteriální obsah hemoglobinu a za předpokladu, že partialpressure O2 v kapilárního řečiště se rovná thePaO2. Pokud je Pao2větší než 150 mmHg, předpokládá se, že veškerý dostupný hemoglobin je nasycený.
pravý zkrat je refrakterní na kyslíkovou terapii., To má za následek to, coje nazýván „refrakterní hypoxémií“. Protože refrakterní hypoxemie nereaguje na kyslíkovou terapii, je třeba hledat jiné prostředkyzlepšit arteriální okysličení. Ty mohou zahrnovat léčbu patologie, aplikaci pozitivní end Expiratoryptlakové terapie (PEEP) nebo zvýšení obsahu kyslíku k udržovánípřijatelné dodávky kyslíku.
nejčastější příčiny refraktoryhypoxémie jsou rozděleny na srdeční a plicní., Nejčastějiplicní příčiny jsou konsolidovaná pneumonitida,atelektáza, novotvar nebo syndrom akutní respirační tísně/akutní plicní onemocnění.
zkrat a PEEP
protože true shunt není citlivý na kyslík, může být na postižené plíce aplikován pozitivní expirační tlak nebo PEEP terapie, aby se snížila QSP/QT. Mezi fyziologické reakce viděn s PEEP jsou lepší okysličení,zvýšení funkční reziduální kapacity, zlepšit plicní complianceand snížení posunování.,
snížení posunovací viděn s PEEPis většina klasicky připisována alveolární recruitment nebo existují ve funkční reziduální kapacita sekundární inflationof dříve se zhroutil sklípků .
Gattinoni popsal pomocí počítačové tomografie regionální distribuci plynu v tkáníchběhem titrace PEEP . Tyto studie potvrdily, žeklasický inflexní bod v křivce plynu / tkáně, což jeodržující alveolárního náboru .
odpověď Peeptitrace se liší nejen typem plicní patologie, ale takés studovanou oblastí plic., Více závislá plic regionsundergo vyšší stupně alveolární recruitment zatímco lessdependent plic regiony mají tendenci mít větší zvyšuje inalveolar objem bez nábor a oblastech plic, které arenon-reagovat na PEEP jsou rovnoměrně rozloženy po celé plíce.
Další metody zlepšení okysličení zahrnují náchylné polohování, což zvyšuje homogenitu intrapulmonálního procesu azlepšuje ventilaci .