læringsmål
- Beskrive den lytiske og lysogenic livscyklus
- Beskrive replikationen af dyr virus
- Beskrive unikke egenskaber af retrovirus og latente virus
- Diskutere menneskelige virus og virus-vært celle interaktioner
- Forklare den proces, transduktion
- Beskrive replikering processen med at plante virus
Alle vira afhænger af celler til reproduktion og metaboliske processer., I sig selv koder vira ikke for alle de en .ymer, der er nødvendige for viral replikation. Men inden for en værtscelle kan en virus kommandere cellulære maskiner til at producere flere virale partikler. Bakteriofager replikerer kun i cytoplasmaet, da prokaryote celler ikke har en kerne eller organeller. I eukaryote celler kan de fleste DNA-vira replikere inde i kernen, med en undtagelse observeret i de store DNA-vira, såsom Po .virus, der kan replikere i cytoplasmaet. RNA-vira, der inficerer dyreceller, replikerer ofte i cytoplasmaet.,
Livscyklus af Vira med Prokaryote Værter
livscyklus bacteriophages har været en god model for forståelsen af hvordan virus påvirker de celler, som de inficerer, da lignende processer er blevet observeret for eukaryote virus, som kan medføre øjeblikkelig død af cellen eller etablere en latent eller kronisk infektion. Virulente fager fører typisk til cellens død gennem cellelyse., Tempererede fager, på den anden side, kan blive en del af et værtskromosom og replikeres med cellegenomet, indtil de induceres til at fremstille nyligt samlede vira, eller afkom-vira.
den lytiske cyklus
under den lytiske cyklus af virulent fag overtager bakteriofagen cellen, gengiver nye fager og ødelægger cellen. T-selv fag er et godt eksempel på en velkarakteriseret klasse af virulente fag. Der er fem trin i den bakteriofaglytiske cyklus (se figur 1)., Vedhæftning er det første trin i infektionsprocessen, hvor Fagen interagerer med specifikke bakterieoverfladereceptorer (f.lipopolysaccharider og ompc-protein på værtsoverflader). De fleste fager har et snævert værtsområde og kan inficere en bakterieart eller en stamme inden for en art. Denne unikke anerkendelse kan udnyttes til målrettet behandling af bakteriel infektion ved fagterapi eller til fagtypning for at identificere unikke bakterielle underarter eller stammer. Den anden fase af infektion er indrejse eller penetration., Dette sker gennem sammentrækning af haleskeden, der fungerer som en hypodermisk nål til at injicere det virale genom gennem cellevæggen og membranen. Faghovedet og de resterende komponenter forbliver uden for bakterierne.

Figur 1. En virulent fag viser kun den lytiske cyklus, der er afbildet her. I den lytiske cyklus replikerer Fagen og lyser værtscellen.
den tredje fase af infektion er biosyntese af nye virale komponenter., Efter indtastning af værtscellen syntetiserer viruset viruskodede endonukleaser for at nedbryde det bakterielle kromosom. Derefter kaprer værtscellen for at replikere, transkribere og oversætte de nødvendige virale komponenter (capsomerer, kappe, bundplader, halefibre og virale en .ymer) til samling af nye vira. Polymerasegener udtrykkes normalt tidligt i cyklussen, mens kapsid-og haleproteiner udtrykkes senere. Under modningsfasen oprettes nye virioner. For at frigøre frie fager forstyrres bakteriecellevæggen af fagproteiner, såsom holin eller Lyso .ym., Det sidste stadium er frigivelse. Modne vira brast ud af værtscellen i en proces kaldet lysis og afkom virus frigøres i miljøet for at inficere nye celler.
den lysogene cyklus
i en lysogen cyklus kommer faggenomet også ind i cellen gennem fastgørelse og penetration. Et godt eksempel på en fag med denne type livscyklus er lambda fag. Under den lysogene cyklus integrerer faggenomet i stedet for at dræbe værten i det bakterielle kromosom og bliver en del af værten. Det integrerede faggenom kaldes en profage., En bakteriel vært med en profage kaldes et lysogen. Processen, hvor en bakterie er inficeret af en tempereret fag, kaldes lysogeni. Det er typisk for tempererede fager at være latent eller inaktiv i cellen. Når bakterien replikerer sit kromosom, replikerer den også fagets DNA og overfører det til nye datterceller under reproduktion. Tilstedeværelsen af fag kan ændre fænotypen af bakterien, da det kan bringe i ekstra gener (f.toksin gener, der kan øge bakteriel virulens)., Denne ændring i værtsfænotypen kaldes lysogen konvertering eller fagkonvertering. Nogle bakterier, såsom Vibrio cholerae og Clostridium botulinum, er mindre virulente i fravær af profagen. De fager, der inficerer disse bakterier, bærer toksingenerne i deres genom og øger virulensen af værten, når toksingenerne udtrykkes. I tilfælde af V. kolera kan fag kodet toksin forårsage alvorlig diarr.; i C. botulinum kan toksinet forårsage lammelse., Under lysogeni vil profagen fortsætte i værtskromosomet indtil induktion, hvilket resulterer i udskæring af det virale genom fra værtskromosomet. Efter induktion kan den tempererede fag fortsætte gennem en lytisk cyklus og derefter gennemgå lysogeni i en nyligt inficeret celle (se figur 2).

Figur 2. En tempereret bakteriofag har både lytiske og lysogene cyklusser. I den lysogene cyklus inkorporeres fag-DNA i værtsgenomet, der danner en profage, der overføres til efterfølgende generationer af celler., Miljømæssige stressfaktorer såsom sult eller eksponering for giftige kemikalier kan få profagen til at blive udskåret og komme ind i den lytiske cyklus.
denne video illustrerer stadierne af den lysogene livscyklus af en bakteriofag og overgangen til en lytisk fase.
tænk over det
- er en latent fag uopdagelig i en bakterie?
transduktion
transduktion opstår, når en bakteriofag overfører bakterielt DNA fra en bakterie til en anden under sekventielle infektioner., Der er to typer transduktion: generaliseret og specialiseret transduktion. Under den lytiske cyklus af viral replikation kaprer viruset værtscellen, nedbryder værtschromosomet og gør flere virale genomer. Når det samles og pakker DNA i faghovedet, gør emballagen lejlighedsvis en fejl. I stedet for at pakke viralt DNA, tager det et tilfældigt stykke vært-DNA og indsætter det i kapsidet. Når den er frigivet, vil denne virion derefter injicere den tidligere værts DNA i en nyligt inficeret vært., Den aseksuelle overførsel af genetisk information kan tillade DNA-rekombination at forekomme, hvilket giver den nye vært nye gener (f.et antibiotikaresistensgen eller et sukkermetaboliserende gen).generaliseret transduktion forekommer, når et tilfældigt stykke bakterielt kromosomalt DNA overføres af Fagen under den lytiske cyklus. Specialiseret transduktion forekommer i slutningen af den lysogene cyklus, når profagen udskæres, og bakteriofagen kommer ind i den lytiske cyklus. Da fag er integreret i værtsgenomet, kan profagen replikere som en del af værten., Ultraviolet lyseksponering eller kemisk eksponering) stimulerer profagen til at gennemgå induktion, hvilket får Fagen til at udskære fra genomet, indtaste den lytiske cyklus og producere nye fager for at forlade værtsceller. Under processen med e .cision fra værtschromosomet kan en fag lejlighedsvis fjerne noget bakterielt DNA nær stedet for viral integration. Fag og vært-DNA fra den ene ende eller begge ender af integrationsstedet pakkes i kapsidet og overføres til den nye inficerede vært., Da DNA ‘ et overført af Fagen ikke er tilfældigt pakket, men i stedet er et specifikt stykke DNA nær integrationsstedet, betegnes denne mekanisme for genoverførsel som specialiseret transduktion (se figur 3). DNA ‘ et kan derefter rekombineres med værtskromosom, hvilket giver sidstnævnte nye egenskaber. Transduktion synes at spille en vigtig rolle i den evolutionære proces af bakterier, hvilket giver dem en mekanisme til aseksuel udveksling af genetisk information.

Figur 3., Dette Flo .diagram illustrerer mekanismen for specialiseret transduktion. En integreret fag udskærer, hvilket medfører et stykke af DNA ‘ et ved siden af dets indsættelsespunkt. Ved reinfektion af en ny bakterie integreres fag-DNA ‘ et sammen med det genetiske materiale, der er erhvervet fra den tidligere vært.
tænk over det
- hvilken fag livscyklus er forbundet med hvilke former for transduktion?,
livscyklus for vira med dyreværter
lytiske dyrevirus følger lignende infektionsstadier som bakteriofager: fastgørelse, penetration, biosyntese, modning og frigivelse (se figur 4). Imidlertid varierer mekanismerne for penetration, nukleinsyrebiosyntese og frigivelse mellem bakterielle og animalske vira. Efter binding til vært receptorer, dyr virus ind via endocytose (engulfment af værtscellen) eller gennem membranen fusion (virale kuvert med værtscellens membran)., Mange vira er vært specifikke, hvilket betyder, at de kun inficere en bestemt type vært; og de fleste vira kun inficere visse typer af celler i væv. Denne specificitet kaldes en vævstropisme. Eksempler på dette er påvist af poliovirus, som udstiller tropisme for væv i hjernen og rygmarven, eller influenza-virus, som har en primær tropisme for luftvejene.

Figur 4. Ved influen .avirusinfektion knytter virale glycoproteiner viruset til en værtsepitelcelle. Som følge heraf er viruset opslugt., Viral RNA og virale proteiner er lavet og samlet i nye virioner, der frigives ved spirende.
Dyrevirus udtrykker ikke altid deres gener ved hjælp af den normale strøm af genetisk information—fra DNA til RNA til protein. Nogle vira har et dsDNA-genom som cellulære organismer og kan følge den normale strømning. Andre kan dog have ssdna, dsRNA eller ssrna genomer. Genomets art bestemmer, hvordan genomet replikeres og udtrykkes som virale proteiner., Hvis et genom er ssDNA, vil værtsen .ymer blive brugt til at syntetisere en anden streng, der er komplementær til genomstrengen, hvilket producerer dsDNA. DsDNA kan nu replikeres, transskriberes og oversættes svarende til vært DNA.
hvis det virale genom er RNA, skal der anvendes en anden mekanisme. Der er tre typer RNA-genom: dsRNA, positiv (+) enkeltstreng (+ssRNA) eller negativ (−) enkeltstrenget RNA (- ssrna). Hvis en virus har et + ssRNA-genom, kan det oversættes direkte for at fremstille virale proteiner. Viral genomic + ssRNA fungerer som cellulær mRNA., Hvis en virus imidlertid indeholder et-ssrna-genom, kan værtsribosomerne ikke oversætte det, før – ssrna replikeres til +ssrna ved viral RNA-afhængig RNA-polymerase (RdRP) (se figur 5). RdRP er bragt ind af virussen og kan bruges til at fremstille +ssRNA fra det originale −ssrna-genom. Den RdRP er også et vigtigt enzym til replikering af dsRNA vira, fordi det bruger den negative del af dobbelt-strenget genom som skabelon til at oprette +ssRNA. De nyligt syntetiserede + ssRNA-kopier kan derefter oversættes med cellulære ribosomer.,
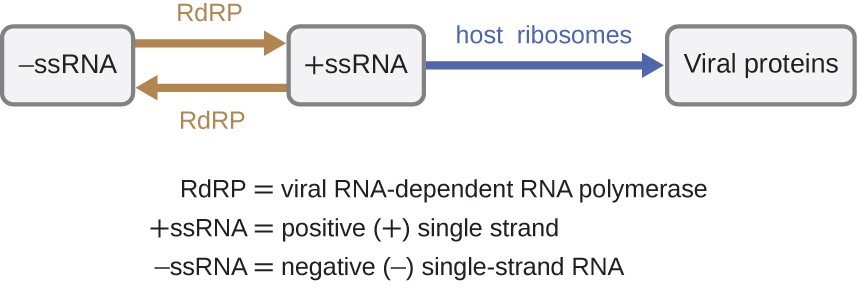
Figur 5. RNA-vira kan indeholde + ssRNA, der kan læses direkte af ribosomerne for at syntetisere virale proteiner. Vira indeholdende – ssrna skal først bruge −ssrna som en skabelon til syntese af +ssrna, før virale proteiner kan syntetiseres.
en alternativ mekanisme til viral nukleinsyresyntese observeres i retroviruserne, som er +ssRNA-vira (se figur 6)., Enkeltstrengede RNA-vira, såsom HIV, bærer et specielt en .ym kaldet revers transkriptase i kapsidet, der syntetiserer en komplementær ssdna (cDNA) – kopi ved hjælp af +ssrna-genomet som en skabelon. SsDNA ‘ en laves derefter til dsDNA, som kan integreres i værtskromosomet og blive en permanent del af værten. Det integrerede virale genom kaldes et provirus. Virusen kan nu forblive i værten i lang tid for at etablere en kronisk infektion. Provirusstadiet ligner profagestadiet i en bakteriel infektion under den lysogene cyklus., I modsætning til profage undergår proviruset imidlertid ikke e .cision efter splejsning i genomet.

Figur 6. Klik for større billede. HIV, et indhyllet, icosahedral retrovirus, bindes til en celleoverfladereceptor af en immuncelle og smelter sammen med cellemembranen. Viralt indhold frigives i cellen, hvor virale en .ymer omdanner det enkeltstrengede RNA-genom til DNA og inkorporerer det i værtsgenomet., (kredit: ændring af arbejde af NIAID, NIH)
tænk over det
- er RNA-afhængig RNA-polymerase fremstillet af et viralt gen eller et værtsgen?
vedvarende infektioner
vedvarende infektion opstår, når en virus ikke er fuldstændigt fjernet fra værtssystemet, men forbliver i visse væv eller organer hos den inficerede person. Virussen kan forblive tavs eller gennemgå produktiv infektion uden alvorligt at skade eller dræbe værten., Mekanismer for vedvarende infektion kan involvere regulering af virale eller værtsgenudtryk eller ændring af værtens immunrespons. De to primære kategorier af vedvarende infektioner er latent infektion og kronisk infektion. Eksempler på virus, der forårsager latente infektioner omfatter herpes simplex virus (mundtlig og genital herpes), varicella-zoster virus (skoldkopper og helvedesild), og Epstein-Barr virus (mononukleose). Hepatitis C-virus og HIV er to eksempler på vira, der forårsager langvarige kroniske infektioner.,
Latent infektion
ikke alle dyrevirus gennemgår replikation ved den lytiske cyklus. Der er vira, der er i stand til at forblive skjult eller sovende inde i cellen i en proces kaldet latenstid. Disse typer af vira er kendt som latente vira og kan forårsage latente infektioner. Virus, der er i stand til latenstid, kan oprindeligt forårsage en akut infektion, før de bliver sovende.for eksempel inficerer varicella-virusoster-viruset mange celler i hele kroppen og forårsager vandkopper, der er karakteriseret ved udslæt af blærer, der dækker huden., Cirka 10 til 12 dage efter infektion opløses sygdommen, og virussen går i dvale og lever inden for nervecelle-ganglier i årevis. I løbet af denne tid dræber virussen ikke nervecellerne eller fortsætter med at replikere. Det er ikke klart, hvorfor den virus stopper gentage i nerve celler og udtrykker par virale proteiner, men, i nogle tilfælde, typisk efter mange år med vækstdvale, virus reaktiveres og forårsager en ny sygdom kaldet helvedesild (Figur 7)., Mens skoldkopper påvirker mange områder i hele kroppen, er helvedesild en nervecelle-specifik sygdom, der kommer ud af ganglierne, hvor virussen var sovende.

Figur 7. (a) Varicella-.oster, den virus, der forårsager skoldkopper, har en indhyllet icosahedral kapsid synlig i denne transmissionselektronmikrograf. Dets dobbeltstrengede DNA-genom bliver inkorporeret i værts-DNA ‘ et. (B) efter en periode med latenstid kan virussen genaktiveres i form af helvedesild, som normalt manifesterer sig som et smertefuldt, lokaliseret udslæt på den ene side af kroppen., (kredit a: ændring af det arbejde, som Erskine Palmer og B. G. Partin—skala-bar data fra Matt Russell; kredit, b: ændring af det arbejde, som Rosmarie Voegtli)
Latent virus kan forblive i dvale af nuværende cirkulære virale genom molekyler uden for værten kromosom. Andre bliver proviruses ved at integrere i værtsgenomet. Under dvale forårsager vira ikke nogen symptomer på sygdom og kan være vanskelige at opdage. En patient kan være uvidende om, at han eller hun bærer virussen, medmindre en viral diagnostisk test er blevet udført.,
kronisk infektion
en kronisk infektion er en sygdom med symptomer, der er tilbagevendende eller vedvarende over lang tid. Nogle virusinfektioner kan være kroniske, hvis kroppen ikke er i stand til at eliminere virussen. HIV er et eksempel på en virus, der producerer en kronisk infektion, ofte efter en lang periode med latenstid. Når en person bliver inficeret med HIV, kan virussen opdages i væv kontinuerligt derefter, men ubehandlede patienter oplever ofte ingen symptomer i årevis., Men virus fastholder kronisk vedholdenhed gennem flere mekanismer, der interfererer med immunfunktion, herunder forebyggelse udtryk for virale antigener på overfladen af de inficerede celler, ændre immunceller sig selv, at begrænse ytringsfriheden af virale gener, og hurtigt skiftende virale antigener gennem mutation. Til sidst resulterer skaden på immunsystemet i progression af sygdommen, der fører til erhvervet immundefekt syndrom (AIDS)., De forskellige mekanismer, som HIV bruger for at undgå at blive ryddet af immunsystemet, bruges også af andre kronisk inficerende vira, herunder hepatitis C-virus.
tænk over det
- på hvilke to måder kan en virus klare at opretholde en vedvarende infektion?
livscyklus for vira med Planteværter
plantevirus ligner mere dyrevirus end bakteriofager. Plantevirus kan være omsluttet eller ikke-omsluttet. Som mange dyrevirus kan plantevirus enten have et DNA-eller RNA-genom og være enkeltstrenget eller dobbeltstrenget., Imidlertid har de fleste plantevirus ikke et DNA-genom; flertallet har et +ssRNA-genom, der fungerer som messenger RNA (mRNA). Kun et mindretal af plantevirus har andre typer genomer.
plantevirus kan have et smalt eller bredt værtsområde. For eksempel inficerer citrus triste virusa-viruset kun nogle få planter af Citrus-slægten, mens agurkmosaikviruset inficerer tusinder af planter af forskellige plantefamilier. De fleste plantevirus overføres ved kontakt mellem planter eller af svampe, nematoder, insekter eller andre leddyr, der fungerer som mekaniske vektorer., Nogle vira kan dog kun overføres af en bestemt type insektvektor; for eksempel kan en bestemt virus overføres af bladlus, men ikke hvide fluer. I nogle tilfælde kan vira også komme ind i sunde planter gennem sår, som kan opstå på grund af beskæring eller vejrskader.
virus, der inficerer planter, betragtes som biotrofiske parasitter, hvilket betyder, at de kan etablere en infektion uden at dræbe værten, svarende til hvad der observeres i bakteriofagernes lysogene livscyklus. Viral infektion kan være asymptomatisk (latent) eller kan føre til celledød (lytisk infektion)., Livscyklussen begynder med virusets indtrængning i værtscellen. Dernæst er viruset ubelagt inden i cytoplasmaet i cellen, når kapsidet fjernes. Afhængigt af typen af nukleinsyre anvendes cellulære komponenter til at replikere det virale genom og syntetisere virale proteiner til samling af nye virioner. For at etablere en systemisk infektion skal viruset komme ind i en del af plantens vaskulære system, såsom phloem. Den tid, der kræves til systemisk infektion, kan variere fra et par dage til et par uger afhængigt af virussen, plantearterne og miljøforholdene., Virussens livscyklus er afsluttet, når den overføres fra en inficeret plante til en sund plante.
tænk over det
- hvad er strukturen og genomet af en typisk plantevirus?
Viral vækstkurve
i modsætning til vækstkurven for en bakteriepopulation følger vækstkurven for en viruspopulation over dens livscyklus ikke en sigmoidal kurve. I den indledende fase forårsager et inokulum af virus infektion. I formørkelsesfasen binder vira og trænger ind i cellerne uden virioner detekteret i mediet., Den største forskel, der Næste vises i den virale vækstkurve sammenlignet med en bakteriel vækstkurve, opstår, når virioner frigives fra den lyserede værtscelle på samme tid. En sådan forekomst kaldes en udbrud, og antallet af virioner pr. I en et-trins multiplikation kurven for bakteriofag, værten celler lyseres, frigive mange virale partikler til mediet, hvilket fører til en meget kraftig stigning i viral titer (antallet af virioner per enhed volumen)., Hvis der ikke er nogen levedygtige værtsceller tilbage, begynder de virale partikler at nedbrydes under kulturens tilbagegang (se figur 8).
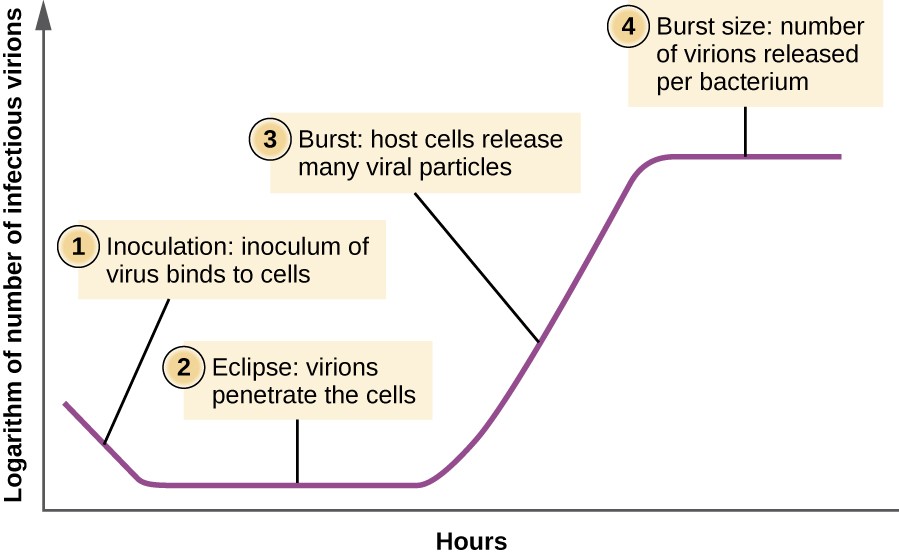
Figur 8. Et-trins multiplikationskurve for en bakteriofagpopulation følger tre trin: 1) inokulering, hvor virionerne knytter sig til værtsceller; 2) formørkelse, hvor indtræden af det virale genom forekommer; og 3) burst, når der produceres tilstrækkeligt antal nye virioner og kommer ud af værtscellen. Burststørrelsen er det maksimale antal virioner produceret pr.,
tænk over det
- hvilket aspekt af en viruss livscyklus fører til den pludselige stigning i vækstkurven?
uregistrerede behandlinger
Ebola er uhelbredelig og dødbringende. Udbruddet i Vestafrika i 2014 var hidtil uset og dværgede andre menneskelige Ebola-epidemier i dødeligheden. Af 24,666 rapporterede eller bekræftede tilfælde døde 10,179 mennesker.
ingen godkendte behandlinger eller vacciner mod Ebola er tilgængelige., Mens nogle lægemidler har vist potentiale i laboratorieundersøgelser og dyremodeller, er de ikke blevet testet hos mennesker for sikkerhed og effektivitet. Ikke alene er disse stoffer uprøvede eller uregistrerede, men de er også en mangelvare.
i betragtning af den store lidelse og høje dødelighed er det rimeligt at spørge, om uregistrerede og uprøvede medicin er bedre end ingen overhovedet. Skal sådanne lægemidler udleveres, og i bekræftende fald hvem skal modtage dem i lyset af deres ekstremt begrænsede forsyninger? Er det etisk at behandle uprøvede lægemidler på patienter med Ebola?, På den anden side er det etisk at tilbageholde potentielt livreddende stoffer fra døende patienter? Eller skal lægemidlerne måske være forbeholdt sundhedsudbydere, der arbejder for at indeholde sygdommen?
i August 2014 blev to inficerede amerikanske hjælpearbejdere og en spansk præst behandlet med .mapp, et uregistreret lægemiddel, der var blevet testet hos aber, men ikke hos mennesker. De to amerikanske hjælpearbejdere kom sig, men præsten døde. Senere samme måned udgav WHOHO en rapport om etikken ved behandling af patienter med lægemidlet., Da Ebola ofte er dødelig, begrundede panelet, at det er etisk at give de uregistrerede stoffer og uetisk at tilbageholde dem af sikkerhedsmæssige bekymringer. Denne situation er et eksempel på “medfølende brug” uden for det veletablerede system for regulering og styring af terapier.
Ebola i OS
På September 24, 2014, Thomas Eric Duncan ankom til Texas Health Presbyterian Hospital i Dallas, der klager over en feber, hovedpine, opkastning og diarré—symptomerne ofte observeret i patienter med forkølelse eller influenza., Efter undersøgelse diagnosticerede en læge på akutafdelingen ham med bihulebetændelse, ordinerede nogle antibiotika og sendte ham hjem. To dage senere vendte Duncan tilbage til hospitalet med ambulance. Hans tilstand var forværret, og yderligere blodprøver bekræftede, at han er blevet inficeret med Ebola-virussen.
yderligere undersøgelser afslørede, at Duncan netop var vendt tilbage fra Liberia, et af landene midt i en alvorlig Ebola-epidemi., Den 15. September, ni dage før han dukkede op på hospitalet i Dallas, havde Duncan hjulpet med at transportere en Ebola-ramt nabo til et hospital i Liberia. Hospitalet fortsatte med at behandle Duncan, men han døde flere dage efter at være blevet indlagt.

Figur 9. Forskere, der arbejder med Ebolavirus, bruger lag af forsvar mod utilsigtet infektion, herunder beskyttelsesbeklædning, åndedrætssystemer og negative lufttrykskabe til bænkarbejde. (kredit: ændring af arbejde af Randal J., Schoepp)
tidslinjen for Duncan-sagen er tegn på Ebolavirusens livscyklus. Inkubationstiden for Ebola varierer fra 2 dage til 21 dage. Ni dage gik mellem Duncans eksponering for virusinfektionen og udseendet af hans symptomer. Dette svarer til dels til formørkelsesperioden i væksten af viruspopulationen. Under formørkelsesfasen ville Duncan ikke have været i stand til at overføre sygdommen til andre. Men når en inficeret person begynder at udvise symptomer, bliver sygdommen meget smitsom., Ebola-virus overføres gennem direkte kontakt med dråber af kropsvæsker som spyt, blod og opkast. Duncan kunne tænkes at have overført sygdommen til andre når som helst, efter at han begyndte at få symptomer, formodentlig nogen tid før hans ankomst til hospitalet i Dallas. Når et hospital indser, at en patient, som Duncan er smittet med Ebola virus, patienten er straks sat i karantæne, og den offentlige sundhed embedsmænd indlede en tilbage spor til at identificere alle, med hvem en patient som Duncan måske har interageret i den periode, hvor han var begyndt at vise symptomer.,
folkesundhedsembedsmænd var i stand til at spore 10 personer med høj risiko (familiemedlemmer til Duncan) og 50 personer med lav risiko for at overvåge dem for tegn på infektion. Ingen fik sygdommen. En af sygeplejerskerne, der var tiltalt for Duncans pleje, blev imidlertid inficeret. Dette sammen med Duncans oprindelige fejldiagnose gjorde det klart, at amerikanske hospitaler var nødt til at yde supplerende uddannelse til medicinsk personale for at forhindre et muligt Ebola-udbrud i USA.
- hvilke typer træning kan forberede sundhedspersonale til at indeholde nye epidemier som Ebola-udbruddet i 2014?,
- hvad er forskellen mellem et smitsomt patogen og et infektiøst patogen?
nøglebegreber og resum Many
- mange vira er målrettet mod specifikke værter eller væv. Nogle kan have mere end en vært.
- mange vira følger flere trin for at inficere værtsceller. Disse faser omfatter vedhæftning, penetration, uncoating, biosyntese, modning og frigivelse.
- bakteriofager har en lytisk eller lysogen cyklus. Den lytiske cyklus fører til værtens død, mens den lysogene cyklus fører til integration af fag i værtsgenomet.,
- bakteriofager injicerer DNA i værtscellen, mens dyrevirus indtræder ved endocytose eller membranfusion.
- Dyrevirus kan gennemgå latenstid, svarende til lysogeni for en bakteriofag.
- størstedelen af plantevirus er ssrna med positiv streng og kan gennemgå latens, kronisk eller lytisk infektion, som observeret for dyrevirus.
- vækstkurven for bakteriofagpopulationer er en multiplikationskurve i et trin og ikke en sigmoidal kurve sammenlignet med bakterievækstkurven.,
- bakteriofager overfører genetisk information mellem værter ved hjælp af enten generaliseret eller specialiseret transduktion.
Multiple Choice
hvilket af følgende fører til ødelæggelsen af værtscellerne?
- lysogenic cyklus
- lytiske cyklus
- prophage
- tempererede fag
en virus opnår sin konvolut i hvilken af følgende faser?,
- vedhæftet fil
- anal
- samling
- slip
hvilke af følgende komponenter bringes ind i en celle af HIV?
- en DNA-afhængig DNA polymerase
- RNA-polymerase
- ribosom
- reverse transkriptase
en RNA-virus med positiv streng:
- skal først konverteres til et mRNA, før det kan oversættes.
- kan bruges direkte til at oversætte virale proteiner.
- nedbrydes af værtsen .ymer.
- genkendes ikke af værts ribosomer.
Hvad hedder overførsel af genetisk information fra en bakterie til en anden bakterie ved en fag?,
- transduktion
- anal
- excision
- oversættelse
tænk over det
- forklar kort forskellen mellem indgangsmekanismen for en T-jævn bakteriofag og et dyrevirus.
- Diskuter forskellen mellem generaliseret og specialiseret transduktion.,
- skelne mellem lytiske og lysogene cyklusser.
- bakteriofager har lytiske og lysogene cyklusser. Diskutere fordele og ulemper for fag.
- Hvordan hjælper revers transkriptase et retrovirus med at etablere en kronisk infektion?
- Diskuter nogle metoder, hvormed plantevirus overføres fra en syg plante til en sund.
- Mærk de fem stadier af en bakteriofaginfektion i figuren:
