Bevezető
Zsírszövet eredetű stroma sejtek (ASCs) vagy multipotens, valamint immunoprivileged, így ideális jelölt terápiás célokra (Bourin et al., 2013; Ma et al., 2014; Kallmeyer and Pepper, 2015). ASCs lehet izolálni minimálisan invazív technikák különböző zsírszövet raktárak a szervezetben (Zuk et al., 2001)., Jellemzőjük, hogy képesek tapadni a műanyaghoz, egy egyedi felületi marker profilhoz, valamint a csont, zsír és porc (Dominici et al., 2006; Bourin et al., 2013). Az ASC-k a zsírszövet stromális vascularis frakciójának (SVF) ~15-30% – át (Bourin et al., 2013; Zuk, 2013), és ki kell bővíteni ex vivo annak érdekében, hogy elegendő sejtszámot kapjunk terápiás célokra.,
biztonságos és szabályozott sejtterápiás termékek biztosítása a betegek számára megköveteli a helyes gyártási gyakorlat (GMP) betartását, és a GMP-irányelveket be kell tartani az ASC-K izolálása, bővítése és differenciálása során (Giancola et al., 2012). Az ASC-k kutatási célokra történő izolálására és kiterjesztésére használt számos reagens állati eredetű vagy nem klinikai minőségű; ezért ezeket a GMP-szabványok szerint megfelelőbb alternatívákkal kell helyettesíteni (Halme and Kessler, 2006; Riis et al., 2015)., Áttekintjük a szérumpótlás választását, amely a magzati szarvasmarha-szérum (FBS) helyett ASC-expanzióra alkalmazható, és leírjuk hatásukat in vitro és in vivo a szakirodalomban leírtak szerint.,
International Society of Cellular Therapy (ISCT) and International Fat Applied Technology Society (IFATS) Guidelines and Techniques Used to assessing Wipose-Derived Stromal Cell Characteries
az International Society of Cellular Therapy (ISCT) és az International Fat Applied Technology Society (IFATS) az ASCs (Dominici et al., 2006; Bourin et al., 2013)., Ezek a kritériumok magukban foglalják az ASC-k műanyaghoz való tapadási képességét, felületi markerprofiljukat és háromoldalú differenciálódási potenciáljukat. A legfrissebb pozíciós tanulmány az életképességet és a proliferációt az eredeti jellemzési kritériumok további méréseként írja le. Ezenkívül kísérleti módszereket és vizsgálatokat határoztak meg a jellemzési kritériumok mérésére (Bourin et al., 2013)., Ezeket a kritériumokat számos tényező befolyásolja, mint például a zsírleszívás technika, az SVF izolációs technika, valamint a tágulási folyamat során alkalmazott média és kiegészítés (Koellensperger et al., 2014; Bajek et al., 2015; Busser et al., 2015). Az ISCT és az IFATS iránymutatásai szerint ajánlott és elfogadott kutatási gyakorlat az egyes izolációs és tenyésztési állapotokra vonatkozó fenti iránymutatások betartásának megerősítése annak érdekében, hogy az így létrejövő sejtpopulációt asc-ként lehessen besorolni.,
Technikák, Módszerek Jellemzik ASCs
Morfológia, Betartását
Egyszer magot, tapadó ASCs kijelző jellegzetes morfológiájú, amely lehet leírni, mint vékony, megnyúlt, orsó alakú. Az ASCs morfológiai értékelését általában fénymikroszkóppal (Trojahn Kølle et al., 2013).
proliferáció
az ISCT és az IFATS irányelvek azt javasolták, hogy a progenitor ACSs proliferációját és gyakoriságát fibroblasztoid kolónia-képző egység vizsgálattal mérjék (Bourin et al., 2013)., Az ebben a felülvizsgálatban említett vizsgálatokban alkalmazott egyéb technikák az életképes sejtek számlálását vagy az ASC-k proliferatív kapacitásának mérését használják immunhisztokémia alkalmazásával. Számolja módszerek közé tartozik a (1) számolva a sejtek segítségével életképességét, festéket, valamint egy hemocytometer, (2) számolva a sejtek segítségével akár számolja gyöngyökkel vagy festési technikák, citometriás analízis, valamint (3) a kolorimetriás vizsgálatok, hogy az intézkedés életképes sejtek spektrofotométer (Gharibi pedig Hughes, 2012; Trojahn Kølle et al., 2013; Bogdanova et al., 2014; Atashi et al., 2015; Johal et al., 2015; Oikonomopoulos et al., 2015).,
Immunofenotípus
az ISCT és az IFATS iránymutatásai a több felületi markerek kifejezését és várható százalékukat határozott követelményként sorolták fel pozíciónyilatkozatukban. Azt is javasolták, hogy a felületi marker expresszióját Többszínű antitestfestéssel (Bourin et al., 2013). Az ebben a felülvizsgálatban végzett vizsgálatok áramlási citometriás elemzést alkalmaztak a felületi marker kifejezés mérésére (Müller et al., 2006; Lindroos et al., 2009; Chieregato et al., 2011; Josh et al., 2012; Trojahn Kølle et al., 2013; Bogdanova et al., 2014; Patrikoski et al., 2014).,
Trilineage Differenciálás
Differenciálás a zsírszövet, csont, porc hagyományosan mérni, hisztokémiai festési technikák láthatóvá alatt mikroszkópia; azonban a ISCT, valamint IFATS iránymutatások javasolta, hogy a minőségi értékelést kell helyettesíteni, vagy kiegészíteni a kvantitatív módszerek, például a mérési vonal-specifikus mrns kifejezés használata reverz transzkripció kvantitatív polimeráz láncreakció (RT-qPCR) technikák (Bourin et al., 2013)., A technikák, amelyeket mérni differenciálás kapacitás, leírt, az idézett tanulmány ebben a felülvizsgálat változatos, a hisztokémiai festés, hagyományos PCR, valamint RT-qPCR. A hisztokémiai festési technikák közé tartozik a sejtek festése (1) olajvörös O-val és nílusvörössel az adipogenezishez; (2) Alizarin vörös S, alkalikus foszfatáz és von Kossa az osteogenezishez; vagy (3) Alcian kék és szafranin a chondrogenezishez (Müller et al., 2006; Kocaoemer et al., 2007; Hebert et al., 2010; Rajala et al., 2010; Koellensperger et al., 2014; Oikonomopoulos et al., 2015; Riis et al., 2016).,
szérum kiegészítés
magzati szarvasmarha szérum
az FBS a sejttenyészetben használt hagyományos szérumkiegészítő. Az FBS in vitro növekedési faktorokat (GFs) és az ASC kötődéséhez, terjeszkedéséhez, fenntartásához és proliferációjához elengedhetetlen egyéb elemeket (Lennon et al., 1995, 1996; Zuk et al., 2001; van der Valk et al., 2010). Az FBS hajlamos a kötegelt variációra, a xenoimmunizációra, valamint a mikoplazmával, vírusokkal, endotoxinokkal és prionokkal való esetleges szennyeződésre (van der Valk et al., 2004, 2010; Chieregato et al., 2011; Kyllonen et al., 2013; Jin et al., 2015)., Az FBS forrása és minősége befolyásolhatja az ASC-k elterjedését és differenciálódását, és fontossá vált a mycoplasma, endotoxinok és vírusok rutinszerű szűrése (Naaijkens et al., 2012). Ezek a tényezők befolyásolhatják a kísérleti eredményeket, és biztonságossá tehetik a sejtterméket klinikai használatra (Zuk et al., 2001; van der Valk et al., 2004; Witzeneder et al., 2013).
az ASC-k immunprivilegatívak, hiányzik a fő hisztokompatibilitási komplex II. osztály, valamint a T és B sejt costimuláló molekulák (CD80, CD86 és CD40) kifejeződése., Az in vitro immunogenitás és immunszuppresszív tulajdonságai ASCs általában mért co-tenyésztés a ASCs a perifériás vér mononukleáris sejtek kevert limfocita reakciók mérése a T-sejt proliferatív válasz (McIntosh et al., 2006; Patrikoski et al., 2014). Az ASC-k immunmoduláló és immunszuppresszív tulajdonságokat mutatnak, amint azt a T-sejt funkció szabályozására és a citokin szekréciójának modulálására in vitro és in vivo (Leto Barone et al., 2013; Roemeling-van Rhijn et al., 2013; Patrikoski et al., 2014)., Ezek a tulajdonságok az ASC-k alacsony immunogenitásából származnak. Az ASC és más mesenchymalis őssejtekkel (MSC) végzett klinikai vizsgálatok többsége (I., II.és III. fázis) FBS-kiegészített táptalajt használ, és beszámoltak arról, hogy az immunogén hatásokat az FBS komponensei váltják ki humán alanyokban (Sundin et al., 2007; Riis et al., 2015). Például az FBS-ben kiterjesztett csontvelőből származó MSCs (BM-MSCs) alkalmazásával végzett klinikai vizsgálat antitesteket talált az FBS komponensei ellen (Horwitz et al., 2002)., Az FBS-re adott immunválaszokról, például Arthus-ról és anafilaxiás reakciókról klinikai vizsgálatokban számoltak be, ahol a betegeket dendritikus sejtekkel és FBS-nek kitett limfocitákkal kezelték (Selvaggi et al., 1997; Mackensen et al., 2000). Ezzel szemben az MSC klinikai vizsgálatok meta-analízise megállapította, hogy a kísérletek több mint 75% – a FBS-t használt sejttágulási protokolljaikban, és csak egy vizsgálatot figyeltek meg és mutattak mellékhatásokat az FBS-re (Lalu et al., 2012)., Az egereknek az ASC-kre adott immunválaszát vizsgáló In vivo vizsgálatok tartósított immunszuppressziót és immunmodulációt, alacsony immunogenitást és az FBS-re adott reakció hiányát mutatták (Cho et al., 2009; González et al., 2009). Bár az ASC-ket széles körben tesztelik a klinikai vizsgálatokban, végleges terápiás szerként történő felhasználásukat továbbra is meg kell határozni. Ezt tovább súlyosbítja a nem biológiailag releváns preklinikai modellek használata (Monsarrat et al., 2016). Továbbá az FBS kevésbé immunogén lehet egerekben és más állatmodellekben, mint az emberekben., Végül az FBS által kiváltott immunválasz (Selvaggi et al., 1997; Mackensen et al., 2000; Horwitz et al., 2002) elképzelhetően befolyásolhatja az átültetett sejtek kilökődését a sejtalapú terápiában.
szérummentes alternatívák
az FBS ismeretlen és meghatározatlan összetétele jelentős hátrány. Előnyös alternatíva lenne egy kémiailag meghatározott közeg, amelynek ismert összetétele van, például a kereskedelemben kapható szérummentes (sf) vagy az XF media (Usta et al., 2014)., Ezeket a szérummentes közegeket tévesen feltételezik, hogy nem tartalmaznak állati eredetű termékeket, mivel az SF és XF kifejezéseket gyakran felcserélhetően használják. Azonban, SF média általában kiegészítik állati eredetű vagy humán szérum albumin és GFS meghatározatlan mennyiségben (Patrikoski et al., 2013). A Xeno – mentes közeg viszont kémiailag meghatározott, meghatározott koncentrációkban jól meghatározott komponenseket tartalmazó közeg (Usta et al., 2014).
növekedési faktorok
a szérum másik alternatívája a GFS hozzáadása a tenyészközeghez, akár elszigetelten, akár koktélként., Ezek a GFs lehet szintetikus, állati eredetű vagy emberi eredetű. A szintetikus GFs-ekkel való helyettesítés előnyösebb a magasabb minőségük és a tételek közötti szabványosítás következtében, ami az állati vagy emberi eredetű GFs esetében nem lehetséges. A leggyakrabban használt GFs a fibroblaszt növekedési faktor, az epidermális növekedési faktor és a vérlemezkéből származó növekedési faktor (PDGF; Baer and Geiger, 2012; Ahearne et al., 2014). A GFs hozzáadása a proliferáció növekedéséhez kapcsolódott (Hebert et al., 2010; Gharibi and Hughes, 2012)., Egy továbbfejlesztett adipogén differenciálódási potenciál korábban számoltak be ASCs bővült GF kiegészített közepes (Hebert et al., 2010). Egy másik tanulmány azonban negatív hatást gyakorolt az adipogén és osteogén differenciálódásra a hosszú távú tenyésztett asc-kben (Gharibi and Hughes, 2012).
szérum Albumin
a szérum albumin bőséges plazmafehérje, amely emberektől és állatoktól izolálható. Gyakran az SF médiát szérumalbuminnal egészítik ki., Összehasonlító vizsgálat a humán szérum albumin az ASC média kiegészítés találtam jobb elterjedése, egy kisebb, orsó -, mint a morfológia, megőrizve differenciálás a zsírszövet, csont, porc (Rajala et al., 2010; Johal et al., 2015).
kémiailag meghatározott XF közeg
Xeno – mentes közeg ajánlott az FBS és a szérum helyettesítésére, mivel tartalmazza az ASC terjeszkedéséhez szükséges komponenseket, nem jár donor-vagy kötegelt variációval, GMP-kompatibilis, minimális immunogenitással és kedvező immunszuppresszióval (van der Valk et al., 2004, 2010; Usta et al.,, 2014). Az FBS-hez képest az XF közeg használata az ASC-k terjeszkedéséhez jobb morfológiai minőséghez, fokozott proliferációhoz, hasonló immunofenotípushoz és differenciálódáshoz vezetett zsír -, csont-és porcszövetekké (Lindroos et al., 2009; Patrikoski et al., 2013; Oikonomopoulos et al., 2015). Az XF média használata az ASC bővítésében azt eredményezi, hogy az ASC-k elveszítik a műanyaghoz való tapadási képességüket (Kyllonen et al., 2013; Patrikoski et al., 2013; Oikonomopoulos et al., 2015). További bevonóanyagokra van szükség az ASC-khez kapcsolódó műanyag-tapadás rejlő jellemzőjének fenntartásához., A kereskedelemben kapható XF medium drága, a házon belüli XF medium elkészítése időigényes lehet, és növelheti a kötegelt variáció kockázatát (Lund et al., 2009; Baer et al., 2010; Rajala et al., 2010; Yang et al., 2012; Kyllonen et al., 2013; Patrikoski et al., 2013; Oikonomopoulos et al., 2015).
emberi alternatívák
az emberi alternatívák helyettesíthetik az FBS-t és az SF / XF-et, és olyan kulturális környezetet hozhatnak létre, amely pontosabban hasonlít az emberi környezetre (Azouna et al., 2012; Koellensperger et al., 2014)., Ezenkívül az autológ (ugyanabból az egyénből származó) termékek használata kiküszöböli a fertőző és más betegséget okozó szerek tesztelésének szükségességét.
humán szérum
miután a teljes vér alvadása antikoaguláns hiányában megtörtént, és centrifugálták, a szérum a kapott folyékony rész, amely nem tartalmaz vérlemezkéket, fehérvérsejteket vagy vörösvérsejteket (1.ábra; Stedman, 2006). A humán szérum (HS) lehet autológ (a donor és a recipiens ugyanaz az egyén) vagy allogén (a recipienstől eltérő személyekből származik)., Mind az autológ, mind az allogén HS felülmúlja az FBS-t (Stute et al., 2004; Bieback et al., 2009, 2012; Bernardo et al., 2011; Kyllonen et al., 2013; Patrikoski et al., 2013). A HS-ben expandált asc-k nagyobb transzkriptóm stabilitással rendelkeznek, mint az FBS-ben expandáltaké, míg a sejtciklus-megnyúlásért, differenciálódásért, extracelluláris mátrixért és prosztaglandin-szintézisért felelős gének az FBS-ben regulálódnak és túlexpresszálódnak a HS-hez képest mikroarray analízissel (Shahdadfar et al., 2005)., Az FBS-ben bővített ASCs hamarabb elérte az öregedést, és telomere rövidülést mutatott a HS-ben kiterjesztett ASCs-hez képest (Shahdadfar et al., 2005). Úgy tűnik, hogy a HS választása kevés hatással van az ASC-k immunmoduláló tulajdonságaira. Az ASC-k az allogén HS-ben vagy a táptalajt tartalmazó FBS-ben alacsony immunogenitást mutattak, és immunszuppressziót eredményeztek (Patrikoski et al., 2014). Az autológ vagy allogén HS-ben kiterjesztett asc-k nagyobb proliferációt és megkülönböztethetetlen immunofenotípust mutatnak az FBS-ben kiterjesztett asc-khez képest (Josh et al., 2012; Bogdanova et al., 2014)., Az allogén HS-ben expandált asc-ket zsír -, csont-és porcszövetekké különböztették meg, bár a chondrogén és osteogén gének upregulációja kedvezett az FBS-hez képest (Josh et al., 2012). ASCs bővült a autológ HS volna differenciált a beavatkozásnak porc; azonban a képesség, hogy differenciálódnak csont volt kevésbé kedvelt (Bogdanova et al., 2014). Az autológ HS az allogén HS-hez (Shahdadfar et al., 2005; Bieback et al., 2009; Bernardo et al., 2011)., Az allogén HS-ben bővülő asc-k növekedési letartóztatásba kerültek, és sejthalálba kerültek (Shahdadfar et al., 2005; Lindroos et al., 2009), amely korlátozza az allogén HS lehetséges előnyeit. Bár az autológ HS ideális lehet, rendelkezésre állása korlátozott, és jelentős eltérések lehetnek a betegek között abban, hogy saját szérumuk képes-e támogatni saját sejtjeik növekedését (Lange et al., 2007). Alternatív megoldásként az allogén HS összevonható, így nagyobb mennyiségeket eredményez a laboratóriumi kísérletekhez, és szigorú minőségvizsgálaton eshet át egy vérbank (pl.,, humán alkalmazás előtt (Bieback et al., 2009).
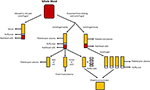
1.ábra. A különböző emberi alternatívák előállítása. A szérumot akkor állítják elő, ha a teljes vér vér vörös-és fehérvérsejtekbe, valamint vérlemezkékbe vérzik és centrifugálják. A plazmát a véralvadás megelőzésével, majd centrifugálással állítják elő., A centrifugálási sebességtől függően vagy vérlemezke-gyenge plazma (PPP; gyors centrifugálás) vagy vérlemezkében gazdag plazma (PRP; lassabb centrifugálás) keletkezik. Ha a PPP -18°C-on tárolódik, akkor friss fagyasztott plazmának nevezik. A thrombocyta koncentrátumok előállíthatók a vérlemezke gyenge plazmájának és 4 buffy rétegének együttes alkalmazásával, vagy több PRP centrifugálásával, valamint a vérlemezke pelletek (kis mennyiségű plazmában szuszpendálva) egyesítésével.,
Plazma
a plazma a vér nem sejtes folyékony része, amely vizet, elektrolitokat és fehérjéket (véralvadási faktorok, fibrinogén és antikoagulánsok) tartalmaz. A vérlemezkék gyenge plazmája( PPP), a friss fagyasztott plazma (FFP) és a vérlemezkében gazdag plazma (PRP; 1.ábra) a teljes vérből különböző sebességgel centrifugálással, majd különböző hőmérsékleten történő tárolással nyerhető. GF szekréció fokozható aktiválásával a vérlemezkék a teljes vérben trombin előtt centrifugálás (Doucet et al., 2005; Kocaoemer et al.,, 2007), ezáltal növelve a plazma termékek aktivitását.
thrombocyta gyenge Plazma
a PPP szinte vérlemezkétől mentes, és a teljes vérből antikoaguláns hozzáadásával állítják elő a gyűjtési folyamat során, majd a plazmát gyors centrifugálással választják el (1. ábra; Koellensperger et al., 2006). Ez lehetővé teszi a vérlemezkék és a vörösvértestek pelletálását. A kapott PPP-t 4°C-on tároljuk, és friss plazmának nevezzük., A PDGF-et az aggregáló vérlemezkék választják ki; azonban a maradék vérlemezkék kis száma miatt elhanyagolható PDGF szabadul fel PPP-ben. Ezért előfordulhat, hogy a GFS-t hozzá kell adni a PPP-hez, ha adathordozón használják, mint az SF medium használatakor (Müller et al., 2006; Gottipamula et al., 2013). A PPP alkalmazása a GFS hozzáadása nélkül alacsonyabb proliferációs rátát és a DNS-szintézis kisebb növekedését eredményezte a timidin-beépítés alkalmazásával mérve, összehasonlítva a HS-vel és az FBS-szel (Vogel et al., 1980; Koellensperger et al., 2006)., PPP hozzáadott GFs eredményezett megnövekedett proliferációs Arány képest HS (Koellensperger et al., 2006); ezek a különbségek azonban a PPP különböző termelési protokolljaiból, valamint a GFs különböző szintjeiből származhattak a jelen tanulmányban szereplő PPP-készítmények mindegyikéhez. Az ASC-K expanziója a PPP-ben jobb proliferációt eredményez az FBS-hez képest, és oszteogén differenciálódást eredményez, amely hasonló a HS-ben kiterjesztett asc-khez (Koellensperger et al., 2014)., Chondrogenic differenciálódás csökkent ASCs bővült PPP képest ASCs bővült PRP (Koellensperger et al., 2014).
friss fagyasztott plazma
az FFP-t ugyanúgy nyerik, mint a PPP-t, de közvetlenül -18°C-on történő elválasztás után fagyasztják (O ‘ Shaughnessy et al., 2004; Liumbruno et al., 2009). Az FFP-t pozitív eredményekkel használták a BM-MSC-k bővítésében., Ezek az eredmények közé tartozik a jobb proliferáció, az immunszuppresszív aktivitás, valamint az adipociták és osteocyták differenciálódása; valamint az FBS-ben kiterjesztett sejtekhez hasonló immunofenotípus és morfológia (Müller et al., 2006; Mannello és Tonti, 2007). Az FFP szérumhelyettesítőként történő alkalmazása az ASC expanzióban azonban további vizsgálatot igényel.
vérlemezkében gazdag plazma
a PRP a vérlemezkékben dúsított vér része. A PRP-t úgy állítják elő, hogy a plazmát a vörösvérsejtektől lassabb Centrifugálási sebességgel elválasztják, ami megakadályozza a vérlemezkék pelletálását (1.ábra)., A PRP-ben kibővült asc-k klasszikus immunofenotípust és morfológiát tartanak fenn, és a PRP növeli a proliferációt az FBS-hez képest (Kocaoemer et al., 2007; Chieregato et al., 2011; Atashi et al., 2015). A PRP-ben bővített asc-k javították a differenciálódási hatékonyságot az adipogén és osteogenikus vonalak felé, miközben összehasonlíthatóak a chondrogén differenciálódás hatékonysága, összehasonlítva az FBS-ben kiterjesztett ASCs-kkel (Kocaoemer et al., 2007; Chieregato et al., 2011). Összehasonlításképpen a HS-t az ASC-k differenciálódása és elterjedése tekintetében valamivel jobbnak találták a PRP-nél (Kocaoemer et al.,, 2007; Chieregato et al., 2011). A PRP a magas biológiai variabilitás és a bonyolult extrakciós eljárás miatt rosszul definiált tápközeg-kiegészítés, amelynek során a vérlemezkefaktorban gazdag felülúszót a plazmamembránokból nehéz lehet megtisztítani. A PRP alkalmazását korlátozza az a nagy mennyiségű teljes vér, amely ahhoz szükséges, hogy elegendő PRP legyen a kísérletezéshez (Chieregato et al., 2011).,
thrombocyta-lizátum
a humán thrombocyta-lizátum (HPL) vérlemezke-GFs-t tartalmaz, amelyeket úgy állítanak elő, hogy a vérlemezkék kis mennyiségű plazmában koncentrálódnak (vérlemezke-koncentrátumok; 1.ábra) hőmérsékleti sokk által. A HPL magasabb GFs-koncentrációt tartalmaz, mint más szérumpótlók, beleértve a humán PRP-t és FBS-t (Doucet et al., 2005; Bernardo et al., 2006, 2011; Bieback et al., 2009; Schallmoser et al., 2010)., A HPL könnyen előállítható és előállítható apheresis termékekből és buffy coats-ból, és reszuszpendálható PRP-ben vagy additív oldatban (Schallmoser and Strunk, 2013; Iudicone et al., 2014). HPL által termelt hideg vérlemezkék között -30 -80°C-on 24 óra, ezt követi egy olvadás, majd centrifugálás lépés. Az ismételt fagyasztási, olvadási és centrifugálási ciklusok lehetővé teszik a GFs felszabadulását és a vérlemezke-testek eltávolítását (Bernardo et al., 2006; Schallmoser et al., 2007)., A HPL-kiegészítés másik előnye, hogy a vérlemezkék a 4-5 napos lejárati idő után használhatók (Bieback et al., 2009). A HPL jobb alternatíva, mint az autológ és allogén HS, mivel a HPL-ben kiterjesztett asc-k fenntartják klasszikus immunofenotípusukat, differenciálódásukat, klonogén hatásfokukat, sejttisztaságukat és sejt életképességüket (Trojahn Kølle et al., 2013; Riis et al., 2016). A HPL támogatja a hosszú távú terjeszkedést anélkül, hogy veszélyeztetné az ASC-k immunmoduláló tulajdonságait, áramlási citometriai elemzéssel mérve (Bieback et al., 2009)., A HPL-ben történő terjeszkedés rövidebb populációs megduplázódást eredményez, csökkentve a sejtbővüléshez szükséges időt, és csökkentve a szeneszcencia és az átalakulás veszélyét (Doucet et al., 2005; Shahdadfar et al., 2005; Bernardo et al., 2006, 2011; Azouna et al., 2012). A HPL biológiai biztonságosságát array comparative genomic hybridization és high sensitivity spectral karyotyping alkalmazásával értékelték, ahol megállapították, hogy a HPL-ben kiterjesztett asc-knek nem volt kromoszómális aberrációja (Crespo-diaz et al., 2011; Trojahn Kølle et al., 2013)., A klasszikus ASC-morfológia (vékony, kisebb, hosszúkás és orsó alakú) a HS-ben és a HPL-ben marad fenn, míg az FBS-ben bővített asc-k nagyobbak és kevésbé orsó alakúak (Trojahn Kølle et al., 2013). Bár ez azt jelezheti, hogy mind a HS, mind a HPL választja a primitív/éretlen asc-ket (Doucet et al., 2005; Bieback et al., 2009), azt is sugallja, hogy az FBS-ben termesztett sejtek csökkentették a proliferációt és gyorsabban haladtak az öregedés felé. A HPL egyénenként változik (Bernardo et al., 2006; Crespo-diaz et al., 2011), valamint a tételenkénti variáció csökken a HPL összevonásakor (Schallmoser et al.,, 2007; Trojahn Kølle et al., 2013). Ezenkívül sok adományozó összevonásával nagy mennyiséget lehet beszerezni kiegészítésre, ami a HPL-t előnyösebbé teszi a PRP-hez (Kocaoemer et al., 2007; Bieback et al., 2009; Chieregato et al., 2011).
következtetés
szerint Riis et al. a kiterjesztett asc-kkel végzett összes regisztrált klinikai vizsgálat közül, amelyek felsorolták bővítési feltételeiket, a többség az FBS-t használja, három vizsgálatban autológ HS-t, egy vizsgálatban PRP-t, egy vizsgálatban pedig HPL-t (Riis et al., 2015)., Ezek a statisztikák riasztóak, mivel az FBS sejttranszplantációt követően képes zoonózisos betegségeket továbbítani, és immunreakciókat jelentettek az FBS komponensekkel szemben (Selvaggi et al., 1997; Mackensen et al., 2000). Az FBS nem GMP-kompatibilis termék, mivel befolyásolja az ASC terápiás alkalmazásának biztonságosságát és hatásosságát, ezért ki kell cserélni (van der Valk et al., 2004; Kyllonen et al., 2013; Witzeneder et al., 2013). Ezt úgy orvosolták, hogy az FBS-t kémiailag meghatározott emberi eredetű alternatívákkal helyettesítették., Változik az FBS emberi alternatívák vagy XF/SF média a regeneratív gyógyászat a fontos előnye, hogy a ASCs szaporodnak, sokkal gyorsabb az utóbbi, ami a nagyobb cellák száma a transzplantáció rövidebb idő alatt. A különböző kulturális média relatív fölényét azonban még mindig széles körben vitatják. Az egynél több táptalajt összehasonlító vizsgálatok különböző eredményeket jelentettek (Lange et al., 2007; Bernardo et al., 2011; Koellensperger et al., 2014; Riis et al., 2016). Koellensperger et al., összehasonlítva a trilineage differenciálás asc bővült FBS, PRP, PPP, és HS (Koellensperger et al., 2014). Eredményeik azt mutatták, hogy minden kultúrközeg lehetővé tette a differenciálást egy vagy több vonalra, de soha nem mindhárom vonalra. Amikor XF media, FBS és HPL kiegészített média összehasonlították, Riis et al. megállapította, hogy bizonyos szubpopulációk a felhasznált tenyészközegtől függően specifikus felületi markereket fejeztek ki (Riis et al., 2016)., Az FBS-ben és a többi tápközegben expandált asc-k immunofenotípusát összehasonlító vizsgálatok a vizsgált markerektől függetlenül alig vagy egyáltalán nem találtak különbséget a sejtfelszíni marker expressziójában (1.táblázat). Vetés sűrűség, oxigén feszültség, összefolyás, disszociáció, és a választás a bazális média is befolyásolhatja a kísérleti eredmények (Sotiropoulou et al., 2006; Freshney, 2010; Bourin et al., 2013; Inamdar and Inamdar, 2013; Feng et al., 2014; Riis et al., 2015)., A tenyészközeg kiválasztása ezen sejtek downstream alkalmazásától (differenciált vagy nem differenciált asc-k alkalmazása) és a kezelendő állapottól függ. Ezenkívül a sejtek klinikai alkalmazás előtti kiterjesztésére használt tenyészközeg immunogenitását olyan paraméternek kell tekinteni, amely befolyásolhatja a klinikai eredményt. A különböző kulturális közegeket összehasonlító legtöbb tanulmány az ISCT és az IFATS által meghatározott kritériumokat használta fel az FBS alternatívájának érvényesítésére., A legtöbb ilyen vizsgálat az ASC morfológiáját, proliferációját, immunofenotípusát, valamint ezen sejtek azon képességét vizsgálja, hogy különbséget tegyenek az osteogén, chondrogén és adipogén vonalak mentén a különböző tenyésztési közegekben. Kevés tanulmány vizsgálta az ASC-k egyéb aspektusait, mint például a szeneszcencia, a genetikai stabilitás, a transzkriptóma, a proteóma, az immunogenitás, a citokin szekréció és a sejtciklus (Shahdadfar et al., 2005; Bieback et al., 2012). Míg az ISCT és az IFATS kritériumai arra törekedtek, hogy egységesítsék a mezőt a szokásos működési eljárások (Dominici et al., 2006; Bourin et al.,, 2013), nincs konszenzus, amely körül az ASC-k tulajdonságai relevánsak a klinikai vizsgálatok szempontjából, így a különböző kulturális médiumok összehasonlítása gyakorlatilag lehetetlen. Míg ezek a kritériumok mérhető eredményeket biztosítanak a könnyű összehasonlításhoz, az ASC-k bővítéséhez használt változó komponensek eltérő hatással lehetnek az ASC végtermékek biztonságosságára, hatékonyságára és reprodukálhatóságára. Az ASC-k transzkriptómában, proteómában és secretome-jában bekövetkezett változások vizsgálata fontos a különböző tápközegekben, csakúgy, mint a megfelelő preklinikai modellekben különböző körülmények között expandált sejtek használata.,

1.táblázat. A különböző média-kiegészítők hatása az ASC-kre in vitro.
szerzői hozzájárulások
CD megfogalmazta és megfogalmazta a felülvizsgálatot, és jóváhagyta a végleges kéziratot. A képviselő támogatta a felülvizsgálat koncepcionalizálását, felülvizsgálta és jóváhagyta a végleges kéziratot. Az MSZP támogatta a felülvizsgálat koncepcióját, szerkesztette és jóváhagyta a végleges kéziratot, és előteremtette az érintett projektek finanszírozását. Minden szerző elolvasta és jóváhagyta a végleges kéziratot.,
finanszírozás
Ez a kutatás és annak közzététele a dél-afrikai Orvosi Kutatási Tanács által nyújtott finanszírozás eredménye a) az MRC zászlóshajói díjak projektje SAMRC-RFA-UFSP-01-2013/őssejtek, valamint (b) az őssejtkutatás és terápia extramurális egysége. A Dél-Afrikai Nemzeti Kutatási Alapítvány szintén finanszírozást nyújtott.
összeférhetetlenségi nyilatkozat
a szerzők kijelentik, hogy a kutatást olyan kereskedelmi vagy pénzügyi kapcsolatok hiányában végezték, amelyek potenciális összeférhetetlenségnek tekinthetők.,
elismerések
a szerzők szeretnék megköszönni Dr. Cheryl Tosh szerkesztői segítségét.
Chieregato, K., Castegnaro, S., Madeo, D., Astori, G., Pegoraro, M., and Rodeghiero, F. (2011). Az epidermális növekedési faktor, a basic fibroblast growth factor és a thrombocyta-derived growth factor-bb helyettesítheti a magzati szarvasmarha szérumot, és versenyezhet a humán vérlemezkében gazdag plazmával a zsírszövetből származó mezenchimális stromális sejtek ex vivo expanziójában. Citoterápia 13, 933-943. doi: 10.3109 / 14653249.2011.,583232
P > PubMed Abstract / CrossRef Full Text / Google Scholar
Mannello, F., and Tonti, G. (2007). Tömör áttekintés: nincs áttörés az emberi mezenchimális és embrionális őssejtkultúrában: kondicionált közeg, feeder réteg vagy feeder-mentes; közepes magzati borjúszérummal, humán szérummal vagy dúsított plazmával; szérummentes, szérum csere nem adagolt közeggel vagy ad hoc formula? minden, ami csillog, nem arany! Őssejtek 25, 1603-1609. doi: 10.1634 / stemcells.2007-0127
P > PubMed Abstract / CrossRef Full Text / Google Scholar
Selvaggi, T. A., Walker, R. E.,, és Fleisher, T. A. (1997). Humán immundeficiencia vírussal fertőzött betegeknél syngeneic lymphocyta infúziókban a magzati borjúszérum elleni antitestek kialakulása arthus-szerű reakciókkal. Vér 89, 776-779.
PubMed Abstract / Google Scholar
Stedman, T. L. (2006). Stedman orvosi szótárában. Philadelphia, PA: Lippincott Williams & Wilkins.
Google Scholar