BEVEZETŐ
Ballon angioplasztika a bal fő koszorúér (LMCA) összefüggésbe a magas eljárási halandóság, valamint gyenge a hosszú távú prognózis.1 ezért a koszorúér bypass műtét a nem védett LMCA léziók kezelésének választása volt, 2 míg az angioplasztikát magas sebészeti kockázati tényezőkkel rendelkező betegek számára fenntartották, és ha sürgős revaszkularizációra van szükség.,3-6 a sztentek és a jobb thrombocyta-gátló szerek bevezetésével a 7 LMCA angioplasztika már nem szigorúan ellenjavallt a kiválasztott betegek sebészeti kezelésének lehetséges alternatívájaként. A jelen tanulmány célja az volt, hogy elemezzük a központunkban kapott azonnali és hosszú távú eredményeket az LMCA angioplasztika segítségével stent implantációval, valamint azonosítsuk a halálozás előrejelzőit.,
betegek és módszer
betegek
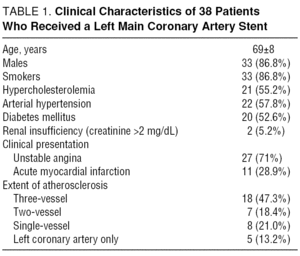
1997 novembere és 2003 márciusa között 2790 beteg közül 38 beteg (33 férfi és 5 nő) 69±8 éves (tartomány, 5085 év), súlyos LMCA elváltozásokkal (1, 36%). Az 1. táblázat összefoglalja a vizsgálati csoport klinikai jellemzőit. A diagnosztikai angiográfia idején 28 betegről (74%) volt ismert, hogy ischaemiás szívbetegségben szenved, hét (18%) korai anginás volt, 3 pedig anginás szívbetegségben szenvedett. Ezekben a betegekben az átlagos bal kamrai ejekciós frakció 49±8% volt., Azonban, 3 betegnél ejekciós frakció
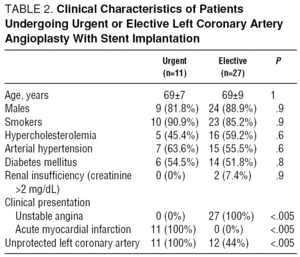
Angioplasztika volt elektív 27 betegek sürgős a fennmaradó 11. Az elektív revaszkularizációt instabil anginára utalták olyan hibás disztális edényekben szenvedő betegeknél, akik nem tudtak ismételt sebészeti beavatkozást végezni, vagy akiknél a műtét kockázata magas volt. A Parsonnet skálája8 szerint a sebészeti kockázat értékeléséhez 16 beteg volt magas kockázatú (pontszám, >18), a fennmaradó 11 pedig alacsony-közepes kockázatú (pontszám, ≤18)., 4 betegnél (10%) a stentet az LMCA eljárási disszekciója miatt ültették be anélkül, hogy veszélyeztetnék a véráramlást. Az elektív kezelésben részesülő betegek csoportjában 1 beteg mutatott enyhe szívelégtelenség klinikai tüneteit. A csoport átesett betegek sürgős kezelést tartalmazza azokat az akut miokardiális infarktus (AMI); 5 (45%) volt a Killip osztály i vagy a II., illetve a fennmaradó 6 (55%) volt a Killip nyha III-IV. A bal koronária keringés volt védtelen 23 betegek (60.5%): 12 (44.4%) a választható kezelési csoport, valamint 11 (100%) a sürgős kezelést csoport.,
az angioplasztika leírása
minden betegnél a hajó a femorális artérián keresztül érhető el. Méret 6 Fr angioplasztika katétereket használtunk. Az eljárás végrehajtása előtt a heparin-nátriumot 100 mg/kg dózisban adták be. 8 betegnél (21%) 0, 25 mg/ttkg abciximab bolust adtak, majd ezt követően folyamatos perfúziót kaptak 12 órán keresztül.
30 beteg (79%) esetében a léziókat egy hagyományos ballonkatéter alkalmazásával predilálták, amelynek átmérője kisebb volt, mint a referenciaszegmensé, és amelyet a szükséges távolság eléréséhez szükséges nyomásra felfújtak., 7 betegnél (18%) a stentet predilatáció nélkül ültették be. 1 betegnél, akiknél súlyosan meszesedett elváltozás volt, szükség volt egy vágó ballon használatára. Ezután a stentet a lézióba helyezték, és miután helyzetét angiográfiával igazolták, a ballont az angioplasztika után
felfújták, 35 beteget 2 thrombocyta-gátló szerrel (azaz acetilszalicilsav tiklopidinnel vagy klopidogréllel) kezeltek. Három, szelepprotézissel rendelkező beteget thrombocyta-gátló szerrel és acenocoumarollal kezeltek., 9 betegnél intraortális ballon ellenpulzációt alkalmaztak.
nyomon követés
minden beteget klinikailag átlagosan 25±20 hónapig (tartomány, 468 hónap) követtek az eljárás után, részletes kihallgatással egy kardiológiai klinikán.,
Meghatározások
Angioplasztika tartották sikeresen befejeződött, amikor a maradék elváltozás volt,
Angiographic Elemzés
A referencia átmérő, a minimális lumen átmérője, valamint a százalékos átmérő stenosis számszerűsítette előtt, illetve után stent implantáció segítségével automatizált digitális angiographic elemzés rendszer alkalmazásával az edge-felismerés (z integris HM3000. Philips Medical Systems, Hollandia).
statisztikai elemzés
statisztikai elemzés a következő számítógépes programok segítségével történt: SPSS version 10 and STATISTICA version 5., Az eredményeket ± standard eltérésekkel fejezzük ki. A kategorikus változók összehasonlítása a χ2 teszt segítségével történt. Kaplan-Meier analízist alkalmaztak a felhalmozódott túlélési valószínűség és a felhalmozódott szív eseménymentes túlélési valószínűség kiszámításához.
eredmények
az angioplasztika minden betegnél sikeres volt. Azonban 1 beteg, aki szívinfarktust kapott a Killip IV. osztályába, és akibe már beültetett egy stentet, meghalt a katerizációs laboratóriumban a nem-reflow jelenség és a szívelégtelenség következtében., Amellett, hogy az LMCA-ba helyezték, a sztenteket 8 betegben (21%), a circumflex artériában 6-ban (15%), mindkét epicardiális artériában 5-ben (13%), A jobb koszorúérben 1-ben (2%) ültették be. Koszorúér-revaszkularizációs műtétre egyetlen beteget sem utaltak.
Mielőtt angioplasztika, az átlagos százalékos átmérőjű szűkület a LMCA 84%±15%; után stent beültetésre, úgy csökkentették, hogy 17%±11% – kal (P
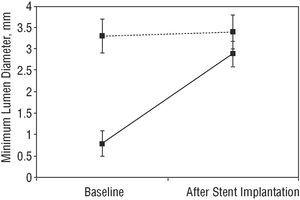
Ábra. 1., A fenti szaggatott vonal mutatja a referencia átmérőt. Az alábbi szilárd vonal szemlélteti a sztentbeültetés által termelt minimális lumenátmérő növekedését.
négy beteg (10%) szenvedett súlyos szövődményeket, amelyek hemodinamikai következmények nélküli, nem transzmurális AMIs-t tartalmaztak.
a kórházi kezelés alatt a mortalitás 15, 8% volt (azaz 38 betegből 6). A sürgős kezelési csoportban 11 betegből 5 (45,4%), akik súlyos szívelégtelenséggel (Killip III.vagy IV. osztály) komplikált AMI-t mutattak be, meghalt a kórházban, szemben a 27 beteg közül 1-vel (3,7%) az elektív kezelési csoportban (P=.,007) (2. ábra). Ez az utolsó beteg, aki a Parsonnet osztályozása szerint alacsony kockázatú volt, tüdővérzés miatt halt meg, amelyet a vérlemezke glikoprotein IIb/IIIa receptor inhibitorokkal történő kezelésnek tulajdonítottak. Nem volt összefüggés a halálozás és az életkor, a nem vagy a cukorbetegség jelenléte között, valószínűleg azért, mert a minta mérete kicsi volt (2.táblázat). Egyetlen beteg sem halt meg a kórházban rosszindulatú aritmia vagy szubakut stent trombózis miatt.
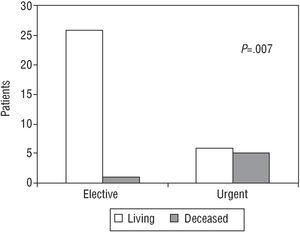
ábra. 2., Halálozás a kórházi kezelés alatt a választható-kezelési és sürgős-kezelési csoportokban.
utánkövetés során 5 beteg (13%) mutatott be jelentősebb klinikai eseményeket. Három, nem védett LMCA-ban szenvedő beteg halt meg: az 2 az angioplasztikát követő első néhány hónapban AMI-t kapott, az 1 pedig hirtelen halált szenvedett. Az 5 beteg közül 2-nél visszatérő anginát mutattak ki, és sikeresen újraszilált. Egyik beteget sem utalták műtétre. Egy másik beteg az angioplasztika után 2 hónappal ischaemiás stroke-ban halt meg.,
elemzése Után, hogy a jelenléte egy szabadalmi bal koronária artéria bypass graft érintett általános szív halálozás, azt találtuk, hogy a 9. 23 beteg (39.1%), aki egy védtelen LMCA meghalt (6 közben kórházi 3 az utánkövetés során). Ezzel szemben a védett LMCA-val rendelkező 15 beteg közül egyik sem halt meg (P=.01).
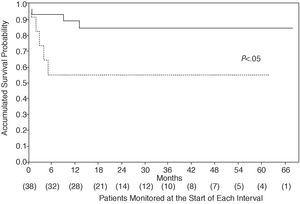
ábra. 3. Felhalmozódott túlélési valószínűség az elektív kezelési csoportban (szilárd vonal) a sürgős kezelési csoporthoz képest (pontozott vonal)., A sürgős kezelés nagyobb mortalitással járt, ami általában az angioplasztikát követő első 6 hónapban fordult elő.
vita
az LMCA hagyományos ballon angioplasztikája fokozott közép – és hosszú távú mortalitással jár. O ‘ Keefe et al sorozat,1 halálozás kezelés során átesett betegeknél választható angioplasztika, aki csinálta vagy nem védett LMCA 4,3% – 9,1% 2 alcsoportok, ill. A 20 hónapos halálozás 65% volt., Hagyományosan tehát a hagyományos LMCA angioplasztika azokra a betegekre korlátozódik, akiknek a műtét magas kockázatú eljárás, valamint azokra, akiknek sürgős kezelésre van szükségük. Ezenkívül a rugalmas visszarúgás jelensége gyakrabban fordul elő az LMCA angioplasztikával, mivel az artériás falak rugalmas rostjai túlsúlyosak.5 a sztentek bevezetése forradalmasította a koszorúér-betegség kezelését, és növelte az LMCA angioplasztikára utaló jelek számát., A sztentek fő jótékony hatásai az, hogy csökkentik az akut elzáródás kockázatát, gátolják az artériás fal rugalmas visszahúzódását, csökkentik a restenosis sebességét.9 a jelen vizsgálatban azt találtuk, hogy az LMCA angioplasztika stent implantációval biztonságos és hatékony eljárás volt a védett LMCA-ban szenvedő, elektív kezelésben részesülő betegeknél. A mortalitás azonban emelkedett azoknál a védtelen LMCA-val rendelkezőknél,akik sürgős beavatkozáson estek át, és akiknél a bal kamrai diszfunkció jelei voltak.,
amint azt más vizsgálatokban megfigyelték, 1013 a jelen vizsgálatban az angioplasztika során az angiográfiás siker aránya 100% volt. Ennek ellenére 1 beteg halt meg AMI és kardiogén sokkban, annak ellenére, hogy az artériát újra szabaddá tették. A mostani sorozatban azt tapasztaltuk, hogy az elektív angioplasztika jó azonnali és hosszú távú eredményekkel jár. Csoportunkban csak 1 beteg halt meg. A halál oka a pulmonalis vérzés volt, amelyet a vérlemezke glikoprotein IIb/IIIa receptor inhibitorokkal történő kezelésnek tulajdonítottak. Az elektív kezelési csoportban a teljes mortalitás 15% volt., A Park et al sorozatában 10, hasonló jellemzőkkel rendelkező, 42 betegből álló, az angina és a restenosis megismétlődési aránya sorrendben 17%, illetve 22% volt. Csak 1 beteg halt meg a koszorúér bypass műtét során, amelyet az in-stent restenosis miatt végeztek. Ezeket a kedvező eredményeket azért kaptuk, mert a vizsgálatban védett LMCA-val és megőrzött kamrai funkcióval rendelkező betegeket vizsgáltak.
sorozatunkban a sürgős kezelésre szoruló csoportban a teljes mortalitás 45% volt., Ez a magas arány azért következett be, mert csoportunk elsősorban olyan betegekből állt, akiket AMI-vel fogadtak be, és akik bizonytalan klinikai állapotban voltak. Fontos megjegyezni, hogy az LMCA minden esetben védtelen volt. Ez a tényező meghatározza mind a rövid távú, mind a hosszú távú prognózist, függetlenül attól, hogy a betegek elektív vagy sürgős kezelésben részesülnek-e.13-15 a sorozatunkban az összes beteg, aki meghalt, védtelen LMCA volt. Ezzel szemben egyetlen, védett LMCA-val rendelkező beteg sem halt meg., Az ULTIMA multicentrikus nyilvántartásban 14, amely 17 beteget tartalmazott, akik az AMI miatt nem védett LMCA-ban stent beültetésen estek át, a kórházi halálozási arány 53% volt, a 12 hónapos halálozási arány vagy a műtét szükségessége 58% volt. Tanulmányunkban az angioplasztikán átesett, súlyos kamrai diszfunkcióval (azaz Killip III. vagy IV. osztályú) rendelkező betegek többsége a sikeres revaszkularizáció ellenére kórházi kezelés alatt halt meg. Ezeknél a betegeknél a halál oka fokozatosan romló szívelégtelenség volt., Egy Ellis et al által nem védett LMCA-ban szenvedő betegeknél végzett multicentrikus vizsgálatban a kamrai diszfunkciót találták a halálozás legfontosabb előrejelzőjének.15 más szerzőkkel egyetértésben,14, 15 megfigyeltük, hogy a betegek ezen alcsoportjában a halálozás incidenciája rövid távon a legmagasabb (azaz
). Az ismételt perkután revaszkularizációs arány 7% volt (azaz 29 beteg közül 2-nél). Más sorozatok jelentésével ellentétben a jelen vizsgálatban 13 beteget nem utaltak műtétre., Fontos azonban hangsúlyozni, hogy restenosis nyilvánul meg, mint a hirtelen halál végzetes AMI a 3 betegek, akik vetettek választható kezelés védtelen LMCA. Következésképpen az LMCA stentekben szenvedő betegeknél tanácsos rendszeresen ellenőrizni klinikai állapotukat az angioplasztika utáni első néhány hónapban. Ezenkívül azt javasolták, hogy az angiographi C vizsgálatokat az angioplasztikát követő 6-16. héten korán kell elvégezni a gyorsan fejlődő restenosis kimutatására.15,16 az angiográfia tényleges előnyeit azonban ebben az összefüggésben nem állapították meg., Az antiproliferatív szerekkel bevont stentek használata, amelyek a közelmúltban váltak elérhetővé a piacon, elősegítheti a szív eseményeinek és revaszkularizációs arányainak csökkentését a nyomon követés során.17,18
a jelen sorozat fő korlátai az, hogy nem randomizált vizsgálat volt, és nem volt angiográfiás követés. Ezenkívül a betegminta kis mérete hozzájárulhatott ahhoz, hogy képtelenek vagyunk azonosítani a rossz prognózist jelző tényezőket, mint például az előrehaladott életkor, a diabetes mellitus jelenléte, az alacsony ejekciós frakció vagy a kiterjedt koszorúér-betegség.,9,19 Bár megállapítások megjelent az orvosi irodalomban, különösen azoknál a betegeknél, akiknél a választható kezelés, ösztönözték növekedése jelzések LMCA angioplasztika, randomizált, kontrollált vizsgálatokra van szükség, mielőtt a technika is ajánlott, mint alternatív kezelés azok számára, anélkül, ellenjavallatok, hogy a műtét. Hangsúlyozni kell, hogy azok a betegek, akik jó jelöltek a revaszkularizációs műtétre, általában jó jelöltek az angioplasztikára is. Ezért gondosan ki kell választani azokat, akiknek az angioplasztika megfelelő., Az elektív angioplasztikán átesett betegeknél az eredmények kedvezőbbek, ha a sérülés nem bifurkált, az LMCA pedig viszonylag hosszú, mint amikor a sérülés egy rövid LMCA-t érint, és magában foglalja a bifurkációt.20 az AMI kardiogén sokkban szenvedő betegeknél az angioplasztika valószínűleg az egyetlen terápiás lehetőség a rossz eredmények ellenére.
összefoglalva, az lmca angioplasztika stent implantációval biztonságos eljárás kiválasztott betegeknél. A védett LMCA-val rendelkező egyének elektív angioplasztikája a súlyos szívbetegségek viszonylag alacsony előfordulási gyakoriságával jár., A sürgős kezelésben részesülő betegek rossz prognózisával kapcsolatos fő kockázati tényezők az AMI, a kamrai diszfunkció klinikai tünetei és a nem védett LMCA.
lásd a szerkesztőséget a 1009-13. oldalon