Lernziele
- Beschreiben Sie die lytischen und lysogenen Lebenszyklen
- Beschreiben Sie den Replikationsprozess von Tierviren
- Beschreiben Sie einzigartige Eigenschaften von Retroviren und latenten Viren
- Diskutieren Sie menschliche Viren und ihre Virus-Wirtszellen-Interaktionen
- Erklären Sie den Transduktionsprozess
- Beschreiben Sie den Replikationsprozess von Pflanzenviren
Alle Viren sind auf Zellen für Fortpflanzungs-und Stoffwechselprozesse angewiesen., Viren selbst kodieren nicht für alle Enzyme, die für die Virusreplikation notwendig sind. Aber innerhalb einer Wirtszelle kann ein Virus die zelluläre Maschinerie befehlen, um mehr Viruspartikel zu produzieren. Bakteriophagen replizieren nur im Zytoplasma, da prokaryotische Zellen keinen Kern oder Organellen haben. In eukaryotischen Zellen können sich die meisten DNA-Viren im Kern replizieren, mit einer Ausnahme, die bei den großen DNA-Viren wie den Poxviren beobachtet wird, die sich im Zytoplasma replizieren können. RNA-Viren, die tierische Zellen infizieren, replizieren sich häufig im Zytoplasma.,
Der Lebenszyklus von Viren mit Prokaryotenwirten
Der Lebenszyklus von Bakteriophagen war ein gutes Modell, um zu verstehen, wie Viren die von ihnen infizierten Zellen beeinflussen, da ähnliche Prozesse für eukaryotische Viren beobachtet wurden, die einen sofortigen Tod der Zelle verursachen oder eine latente oder chronische Infektion verursachen können. Virulente Phagen führen typischerweise zum Tod der Zelle durch Zelllyse., Gemäßigte Phagen hingegen können Teil eines Wirtschromosoms werden und werden mit dem Zellgenom repliziert, bis sie zu neu zusammengesetzten Viren oder Nachkommenschaftsviren induziert werden.
Der lytische Zyklus
Während des lytischen Zyklus des virulenten Phagen übernimmt der Bakteriophage die Zelle, reproduziert neue Phagen und zerstört die Zelle. T-even Phage ist ein gutes Beispiel für eine gut charakterisierte Klasse virulenter Phagen. Es gibt fünf Stufen im Bakteriophagen-lytischen Zyklus (siehe Abbildung 1)., Die Anheftung ist die erste Stufe des Infektionsprozesses, in der der Phage mit spezifischen bakteriellen Oberflächenrezeptoren (z. B. Lipopolysacchariden und OmpC-Protein auf Wirtsoberflächen) interagiert. Die meisten Phagen haben einen engen Wirtsbereich und können eine Bakterienart oder einen Stamm innerhalb einer Spezies infizieren. Diese einzigartige Erkennung kann zur gezielten Behandlung bakterieller Infektionen durch Phagentherapie oder zur Phagentypisierung zur Identifizierung einzigartiger bakterieller Unterarten oder Stämme genutzt werden. Das zweite Stadium der Infektion ist der Eintritt oder die Penetration., Dies geschieht durch Kontraktion der Schwanzhülle, die wie eine hypodermische Nadel wirkt, um das virale Genom durch die Zellwand und Membran zu injizieren. Der Phagenkopf und die restlichen Komponenten bleiben außerhalb der Bakterien.

Abbildung 1. Ein virulenter Phage zeigt nur den hier abgebildeten lytischen Zyklus. Im lytischen Zyklus repliziert und lysiert der Phage die Wirtszelle.
Die dritte Infektionsstufe ist die Biosynthese neuer Viruskomponenten., Nach dem Eintritt in die Wirtszelle synthetisiert das Virus viruskodierte Endonukleasen, um das bakterielle Chromosom abzubauen. Es entführt dann die Wirtszelle, um die notwendigen viralen Komponenten (Kapsomere, Hüllen, Grundplatten, Schwanzfasern und virale Enzyme) für die Montage neuer Viren zu replizieren, zu transkribieren und zu übersetzen. Polymerase-Gene werden normalerweise früh im Zyklus exprimiert, während Capsid-und Schwanzproteine später exprimiert werden. Während der Reifungsphase werden neue Virionen erzeugt. Um freie Phagen freizusetzen, wird die bakterielle Zellwand durch Phagenproteine wie Holin oder Lysozym gestört., Die letzte Stufe ist die Freigabe. Reife Viren platzen aus der Wirtszelle in einem Prozess namens Lyse und die Nachkommenschaftsviren werden in die Umgebung freigesetzt, um neue Zellen zu infizieren.
Der lysogene Zyklus
In einem lysogenen Zyklus gelangt das Phagen-Genom auch durch Anheftung und Penetration in die Zelle. Ein Paradebeispiel für eine Phage mit dieser Art von Lebenszyklus ist die Lambda-Phage. Während des lysogenen Zyklus integriert sich das Phagen-Genom in das bakterielle Chromosom und wird Teil des Wirts, anstatt den Wirt zu töten. Das integrierte Phagen-Genom wird Prophage genannt., Ein bakterieller Wirt mit einer Prophage wird Lysogen genannt. Der Prozess, bei dem ein Bakterium mit einem gemäßigten Phagen infiziert wird, wird Lysogenie genannt. Es ist typisch für gemäßigte Phagen, latent oder inaktiv in der Zelle zu sein. Da das Bakterium sein Chromosom repliziert, repliziert es auch die DNA des Phagen und gibt sie während der Fortpflanzung an neue Tochterzellen weiter. Das Vorhandensein des Phagen kann den Phänotyp des Bakteriums verändern, da es zusätzliche Gene einbringen kann (z. B. Toxingene, die die bakterielle Virulenz erhöhen können)., Diese Veränderung des Wirt-Phänotyps wird als lysogene Umwandlung oder Phagenkonvertierung bezeichnet. Einige Bakterien, wie Vibrio cholerae und Clostridium botulinum, sind in Abwesenheit der Prophage weniger virulent. Die Phagen, die diese Bakterien infizieren, tragen die Toxingene in ihrem Genom und verstärken die Virulenz des Wirts, wenn die Toxingene exprimiert werden. Bei V. cholera kann phagencodiertes Toxin schweren Durchfall verursachen; Bei C. botulinum kann das Toxin Lähmungen verursachen., Während der Lysogenese bleibt die Prophage bis zur Induktion im Wirtschromosom bestehen, was zur Exzision des viralen Genoms aus dem Wirtschromosom führt. Nach Induktion kann der gemäßigte Phage einen lytischen Zyklus durchlaufen und dann in einer neu infizierten Zelle lysogenisiert werden (siehe Abbildung 2).

Abbildung 2. Ein gemäßigter Bakteriophage hat sowohl lytische als auch lysogene Zyklen. Im lysogenen Zyklus wird Phagen-DNA in das Wirtsgenom integriert und bildet eine Prophage, die an nachfolgende Zellgenerationen weitergegeben wird., Umweltstressoren wie Hunger oder Exposition gegenüber toxischen Chemikalien können dazu führen, dass die Prophage ausgeschnitten wird und in den lytischen Zyklus eintritt.
Dieses Video zeigt die Stadien des lysogenen Lebenszyklus eines Bakteriophagen und den Übergang in eine lytische Phase.
Denken Sie darüber nach
- Ist ein latenter Phage in einem Bakterium nicht nachweisbar?
Transduktion
Transduktion tritt auf, wenn ein Bakteriophage während sequentieller Infektionen bakterielle DNA von einem Bakterium auf ein anderes überträgt., Es gibt zwei Arten der Transduktion: generalisierte und spezialisierte Transduktion. Während des lytischen Zyklus der Virusreplikation entführt das Virus die Wirtszelle, baut das Wirtschromosom ab und bildet mehr virale Genome. Wenn es DNA in den Phagenkopf einfügt und verpackt, macht das Verpacken gelegentlich einen Fehler. Anstatt virale DNA zu verpacken, nimmt es ein zufälliges Stück Wirts-DNA und fügt es in das Kapsid ein. Nach der Freisetzung injiziert dieses Virion die DNA des ehemaligen Wirts in einen neu infizierten Wirt., Die asexuelle Übertragung genetischer Informationen kann eine DNA-Rekombination ermöglichen, wodurch dem neuen Wirt neue Gene (z. B. ein Antibiotikaresistenzgen oder ein zuckermetabolisierendes Gen) zur Verfügung gestellt werden.
Eine generalisierte Transduktion tritt auf, wenn ein zufälliges Stück bakterieller chromosomaler DNA während des lytischen Zyklus vom Phagen übertragen wird. Die spezialisierte Transduktion erfolgt am Ende des lysogenen Zyklus, wenn die Prophage ausgeschnitten wird und der Bakteriophage in den lytischen Zyklus eintritt. Da der Phage in das Wirtsgenom integriert ist, kann sich der Prophage als Teil des Wirts replizieren., Einige Bedingungen (z. B. ultraviolettes Licht oder chemische Exposition) stimulieren jedoch die Induktion des Phagen, wodurch der Phage aus dem Genom ausgeschnitten wird, in den lytischen Zyklus eintritt und neue Phagen erzeugt werden, die Wirtszellen verlassen. Während des Exzisionsvorgangs aus dem Wirtschromosom kann ein Phage gelegentlich bakterielle DNA in der Nähe der Stelle der Virusintegration entfernen. Die Phagen-und Host-DNA von einem Ende oder beiden Enden der Integrationsstelle werden innerhalb des Capsids verpackt und auf den neuen, infizierten Host übertragen., Da die vom Phagen übertragene DNA nicht zufällig verpackt ist, sondern ein spezifisches Stück DNA in der Nähe der Integrationsstelle ist, wird dieser Mechanismus des Gentransfers als spezialisierte Transduktion bezeichnet (siehe Abbildung 3). Die DNA kann dann mit dem Wirtschromosom rekombinieren, was dem letzteren neue Eigenschaften verleiht. Die Transduktion scheint eine wichtige Rolle im Evolutionsprozess von Bakterien zu spielen und gibt ihnen einen Mechanismus für den asexuellen Austausch genetischer Informationen.

Abbildung 3., Dieses Flussdiagramm veranschaulicht den Mechanismus der spezialisierten Transduktion. Ein integrierter Phage schneidet ab und bringt ein Stück der DNA mit, das an seine Einfügemarke angrenzt. Bei der Reinfektion eines neuen Bakteriums integriert sich die Phagen-DNA zusammen mit dem genetischen Material, das vom vorherigen Wirt erworben wurde.
Denken Sie darüber nach
- Welcher Phagen-Lebenszyklus ist mit welchen Transduktionsformen verbunden?,
Lebenszyklus von Viren mit tierischen Wirten
Lytische Tierviren folgen ähnlichen Infektionsstadien wie Bakteriophagen: Anheftung, Penetration, Biosynthese, Reifung und Freisetzung (siehe Abbildung 4). Die Mechanismen der Penetration, Nukleinsäure-Biosynthese und Freisetzung unterscheiden sich jedoch zwischen bakteriellen und tierischen Viren. Nach der Bindung an Wirtsrezeptoren treten tierische Viren durch Endozytose (Verschlingen durch die Wirtszelle) oder durch Membranfusion (Virushülle mit der Wirtszellmembran) ein., Viele Viren sind wirtsspezifisch, was bedeutet, dass sie nur eine bestimmte Art von Wirt infizieren; und die meisten Viren infizieren nur bestimmte Arten von Zellen in Geweben. Diese Spezifität wird als Gewebetrophismus bezeichnet. Beispiele dafür zeigen das Poliovirus, das einen Tropismus für das Gewebe des Gehirns und des Rückenmarks aufweist, oder das Influenzavirus, das einen primären Tropismus für die Atemwege aufweist.

Abbildung 4. Bei der Influenzavirusinfektion binden virale Glykoproteine das Virus an eine Wirtsepithelzelle. Infolgedessen ist das Virus verschlungen., Virale RNA und virale Proteine werden hergestellt und zu neuen Virionen zusammengesetzt, die durch Knospen freigesetzt werden.
Tierische Viren exprimieren ihre Gene nicht immer unter Verwendung des normalen Flusses genetischer Informationen-von DNA über RNA bis Protein. Einige Viren haben ein dsDNA-Genom wie zelluläre Organismen und können dem normalen Fluss folgen. Andere können jedoch ssDNA -, dsRNA-oder ssRNA-Genome aufweisen. Die Art des Genoms bestimmt, wie das Genom repliziert und als virale Proteine exprimiert wird., Wenn ein Genom ssDNA ist, werden Wirtsenzyme verwendet, um einen zweiten Strang zu synthetisieren, der komplementär zum Genomstrang ist, wodurch dsDNA produziert wird. Die dsDNA kann nun ähnlich wie Host-DNA repliziert, transkribiert und übersetzt werden.
Wenn das virale Genom RNA ist, muss ein anderer Mechanismus verwendet werden. Es gibt drei Arten von RNA-Genom: dsRNA, positive ( + ) Einzelstrang (+ssRNA) oder negative (-) Einzelstrang − RNA (- ssRNA). Wenn ein Virus ein +ssRNA-Genom hat, kann es direkt übersetzt werden, um virale Proteine herzustellen. Virale genomische + ssRNA wirkt wie zelluläre mRNA., Wenn ein Virus jedoch ein −ssRNA-Genom enthält, können die Wirtsribosomen es erst übersetzen, wenn die −ssRNA durch virale RNA-abhängige RNA-Polymerase (RdRp) in +ssRNA repliziert wird (siehe Abbildung 5). Das RdRp wird durch das Virus eingebracht und kann verwendet werden, um +ssRNA aus dem Original −ssRNA-Genom herzustellen. Das RdRp ist auch ein wichtiges Enzym für die Replikation von dsRNA-Viren, da es den negativen Strang des doppelsträngigen Genoms als Vorlage verwendet, um +ssRNA zu erzeugen. Die neu synthetisierten + ssRNA-Kopien können dann durch zelluläre Ribosomen übersetzt werden.,
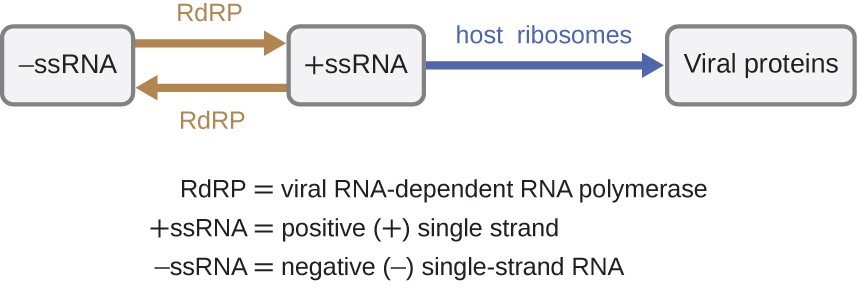
Abbildung 5. RNA-Viren können +ssRNA enthalten, die direkt von den Ribosomen gelesen werden können, um virale Proteine zu synthetisieren. Viren, die −ssRNA enthalten, müssen zuerst die −ssRNA als Vorlage für die Synthese von +ssRNA verwenden, bevor virale Proteine synthetisiert werden können.
Ein alternativer Mechanismus für die virale Nukleinsäuresynthese wird in den Retroviren beobachtet, die +ssRNA-Viren sind (siehe Abbildung 6)., Einzelsträngige RNA-Viren wie HIV tragen ein spezielles Enzym namens Reverse Transkriptase innerhalb des Kapsids, das eine komplementäre ssDNA (cDNA) – Kopie unter Verwendung des +ssRNA-Genoms als Vorlage synthetisiert. Die ssDNA wird dann in dsDNA umgewandelt, die sich in das Wirtschromosom integrieren und ein permanenter Teil des Wirts werden kann. Das integrierte virale Genom wird als Provirus bezeichnet. Das Virus kann jetzt lange im Wirt bleiben, um eine chronische Infektion festzustellen. Das Stadium des Provirus ähnelt dem Stadium der Prophage bei einer bakteriellen Infektion während des lysogenen Zyklus., Im Gegensatz zur Prophage wird das Provirus jedoch nach dem Spleißen in das Genom nicht exzidiert.

Abbildung 6. Klicken Sie für ein größeres Bild. HIV, ein umhülltes, ikosaedrisches Retrovirus, bindet an einen Zelloberflächenrezeptor einer Immunzelle und verschmilzt mit der Zellmembran. Virale Inhalte werden in die Zelle freigesetzt, wo virale Enzyme das einzelsträngige RNA-Genom in DNA umwandeln und in das Wirtsgenom integrieren., (credit: Modifikation der Arbeit durch NIAID, NIH)
Denken Sie darüber nach
- Ist RNA-abhängige RNA-Polymerase aus einem viralen Gen oder einem Wirtsgen?
Persistente Infektionen
Eine persistente Infektion tritt auf, wenn ein Virus nicht vollständig aus dem System des Wirts entfernt wird, sondern in bestimmten Geweben oder Organen der infizierten Person verbleibt. Das Virus kann schweigen oder sich einer produktiven Infektion unterziehen, ohne den Wirt ernsthaft zu schädigen oder zu töten., Mechanismen einer persistierenden Infektion können die Regulation der viralen oder Wirtsgenexpressionen oder die Veränderung der Wirtsimmunantwort beinhalten. Die beiden Hauptkategorien persistierender Infektionen sind latente Infektionen und chronische Infektionen. Beispiele für Viren, die latente Infektionen verursachen, sind Herpes-simplex-Virus (oraler und genitaler Herpes), Varicella-Zoster-Virus (Windpocken und Gürtelrose) und Epstein-Barr-Virus (Mononukleose). Hepatitis-C-Virus und HIV sind zwei Beispiele für Viren, die langfristige chronische Infektionen verursachen.,
Latente Infektion
Nicht alle tierischen Viren werden durch den lytischen Zyklus repliziert. Es gibt Viren, die in der Lage sind, in einem Prozess namens Latenz in der Zelle verborgen oder ruhend zu bleiben. Diese Arten von Viren sind als latente Viren bekannt und können latente Infektionen verursachen. Viren, die latenzfähig sind, können zunächst eine akute Infektion verursachen, bevor sie inaktiv werden.
Zum Beispiel infiziert das Varicella-Zoster-Virus viele Zellen im ganzen Körper und verursacht Windpocken, die durch einen Blasenausschlag gekennzeichnet sind, der die Haut bedeckt., Etwa 10 bis 12 Tage nach der Infektion löst sich die Krankheit auf und das Virus schläft und lebt jahrelang in Nervenzellganglien. Während dieser Zeit tötet das Virus die Nervenzellen nicht ab oder repliziert sich weiter. Es ist nicht klar, warum das Virus innerhalb der Nervenzellen nicht mehr repliziert und nur wenige virale Proteine exprimiert, aber in einigen Fällen wird das Virus typischerweise nach vielen Jahren der Ruhe reaktiviert und verursacht eine neue Krankheit namens Gürtelrose (Abbildung 7)., Während Windpocken viele Bereiche im ganzen Körper betreffen, ist Gürtelrose eine nervenzellspezifische Erkrankung, die aus den Ganglien austritt, in denen das Virus ruhte.

Abbildung 7. (a) Varicella-Zoster, das Virus, das Windpocken verursacht, hat ein umhülltes ikosaedrisches Kapsid, das in diesem Transmissionselektronenmikrographen sichtbar ist. Sein doppelsträngiges DNA-Genom wird in die Wirts-DNA integriert. (b) Nach einer Latenzzeit kann sich das Virus in Form von Gürtelrose reaktivieren, was sich normalerweise als schmerzhafter, lokalisierter Hautausschlag auf einer Körperseite manifestiert., (credit a: Änderung der Arbeit von Erskine Palmer und B. G. Partin-Scale-bar-Daten von Matt Russell; credit b: Änderung der Arbeit von Rosmarie Voegtli)
Latente Viren können ruhen, indem sie als zirkuläre virale Genommoleküle außerhalb des Wirt-Chromosoms existieren. Andere werden durch die Integration in das Wirtsgenom zu Proviren. Während der Ruhezeit verursachen Viren keine Krankheitssymptome und können schwer zu erkennen sein. Ein Patient kann sich nicht bewusst sein, dass er oder sie das Virus trägt, es sei denn, ein viraler diagnostischer Test wurde durchgeführt.,
Chronische Infektion
Eine chronische Infektion ist eine Krankheit mit Symptomen, die über einen langen Zeitraum wiederkehrend oder anhaltend sind. Einige Virusinfektionen können chronisch sein, wenn der Körper das Virus nicht beseitigen kann. HIV ist ein Beispiel für ein Virus, das eine chronische Infektion hervorruft, oft nach einer langen Latenzzeit. Sobald eine Person mit HIV infiziert ist, kann das Virus danach kontinuierlich im Gewebe nachgewiesen werden, aber unbehandelte Patienten haben oft jahrelang keine Symptome., Das Virus behält jedoch eine chronische Persistenz durch mehrere Mechanismen bei, die die Immunfunktion beeinträchtigen, einschließlich der Verhinderung der Expression viraler Antigene auf der Oberfläche infizierter Zellen, der Veränderung der Immunzellen selbst, der Einschränkung der Expression viraler Gene und der schnellen Veränderung viraler Antigene durch Mutation. Schließlich führt die Schädigung des Immunsystems zum Fortschreiten der Krankheit, die zum erworbenen Immunschwächesyndrom (AIDS) führt., Die verschiedenen Mechanismen, mit denen HIV verhindert, dass es vom Immunsystem gelöscht wird, werden auch von anderen chronisch infizierenden Viren, einschließlich des Hepatitis-C-Virus, eingesetzt.
Denken Sie darüber nach
- Auf welche zwei Arten kann ein Virus eine anhaltende Infektion aufrechterhalten?
Lebenszyklus von Viren mit Pflanzenwirten
Pflanzenviren sind tierischen Viren ähnlicher als Bakteriophagen. Pflanzenviren können umhüllt oder nicht umhüllt sein. Wie viele tierische Viren können Pflanzenviren entweder ein DNA – oder RNA-Genom haben und einzelsträngig oder doppelsträngig sein., Die meisten Pflanzenviren haben jedoch kein DNA-Genom; Die Mehrheit hat ein + ssRNA-Genom, das wie Messenger-RNA (mRNA) wirkt. Nur eine Minderheit der Pflanzenviren hat andere Arten von Genomen.
Pflanzenviren können einen engen oder breiten Wirtsbereich haben. Zum Beispiel infiziert das Citrus Tristeza Virus nur wenige Pflanzen der Citrus Gattung, während das Gurkenmosaikvirus Tausende von Pflanzen verschiedener Pflanzenfamilien infiziert. Die meisten Pflanzenviren werden durch Kontakt zwischen Pflanzen oder durch Pilze, Nematoden, Insekten oder andere Arthropoden, die als mechanische Vektoren wirken, übertragen., Einige Viren können jedoch nur durch eine bestimmte Art von Insektenvektor übertragen werden; Zum Beispiel kann ein bestimmtes Virus durch Blattläuse, aber nicht durch weiße Fliegen übertragen werden. In einigen Fällen können Viren auch durch Wunden in gesunde Pflanzen eindringen, wie dies durch Schnitt-oder Wetterschäden auftreten kann.
Viren, die Pflanzen infizieren, gelten als biotrophe Parasiten, was bedeutet, dass sie eine Infektion feststellen können, ohne den Wirt zu töten, ähnlich wie dies in den lysogenen Lebenszyklen von Bakteriophagen beobachtet wird. Eine Virusinfektion kann asymptomatisch (latent) oder zum Zelltod (lytische Infektion) führen., Der Lebenszyklus beginnt mit dem eindringen des virus in die Wirtszelle. Als nächstes wird das Virus innerhalb des Zytoplasmas der Zelle unbeschichtet, wenn das Kapsid entfernt wird. Abhängig von der Art der Nukleinsäure werden zelluläre Komponenten verwendet, um das virale Genom zu replizieren und virale Proteine für die Montage neuer Virionen zu synthetisieren. Um eine systemische Infektion festzustellen, muss das Virus in einen Teil des Gefäßsystems der Pflanze wie das Phloem eindringen. Die für eine systemische Infektion erforderliche Zeit kann je nach Virus, Pflanzenart und Umweltbedingungen zwischen einigen Tagen und einigen Wochen variieren., Der Lebenszyklus des Virus ist abgeschlossen, wenn es von einer infizierten Pflanze auf eine gesunde Pflanze übertragen wird.
Denken Sie darüber nach
- Was ist die Struktur und das Genom eines typischen Pflanzenvirus?
Virale Wachstumskurve
Im Gegensatz zur Wachstumskurve für eine Bakterienpopulation folgt die Wachstumskurve für eine Viruspopulation über ihren Lebenszyklus keiner sigmoidalen Kurve. Während der Anfangsphase verursacht ein Inokulum des Virus eine Infektion. In der Eclipse-Phase binden und durchdringen Viren die Zellen, ohne dass Virionen im Medium nachgewiesen werden., Der Hauptunterschied, der als nächstes in der viralen Wachstumskurve im Vergleich zu einer bakteriellen Wachstumskurve auftritt, tritt auf, wenn Virionen gleichzeitig aus der lysierten Wirtszelle freigesetzt werden. Ein solches Auftreten wird als Burst bezeichnet, und die Anzahl der Virionen pro freigesetztem Bakterium wird als Burst-Größe beschrieben. In einer einstufigen Multiplikationskurve für Bakteriophagen lysieren die Wirtszellen und setzen viele Viruspartikel in das Medium frei, was zu einem sehr steilen Anstieg des Virustiters (der Anzahl der Virionen pro Volumeneinheit) führt., Wenn keine lebensfähigen Wirtszellen verbleiben, beginnen sich die Viruspartikel während des Niedergangs der Kultur abzubauen (siehe Abbildung 8).
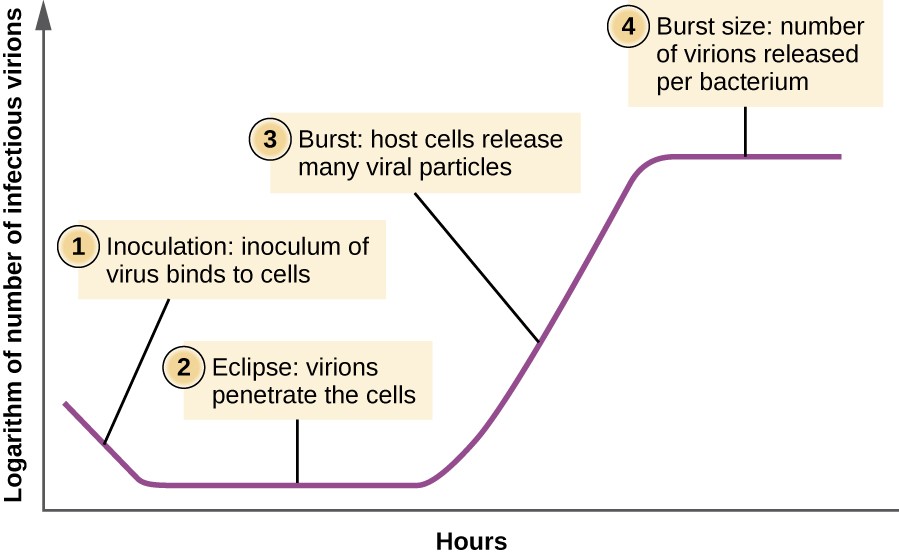
Abbildung 8. Die einstufige Multiplikationskurve für eine Bakteriophagenpopulation folgt drei Schritten: 1) Impfung, bei der sich die Virionen an Wirtszellen anlagern; 2) Eclipse, bei der der Eintritt des viralen Genoms auftritt; und 3) Burst, wenn eine ausreichende Anzahl neuer Virionen produziert wird und aus der Wirtszelle austritt. Die Burstgröße ist die maximale Anzahl von Virionen, die pro Bakterium produziert werden.,
Denken Sie darüber nach
- Welcher Aspekt des Lebenszyklus eines Virus führt zu einem plötzlichen Anstieg der Wachstumskurve?
Nicht registrierte Behandlungen
Ebola ist unheilbar und tödlich. Der Ausbruch in Westafrika im Jahr 2014 war beispiellos und stellte andere menschliche Ebola-Epidemien in den Schatten. Von 24.666 gemeldeten Verdachtsfällen oder bestätigten Fällen starben 10.179 Menschen.
Es sind keine zugelassenen Behandlungen oder Impfstoffe gegen Ebola verfügbar., Während einige Medikamente in Laborstudien und Tiermodellen Potenzial gezeigt haben, wurden sie beim Menschen nicht auf Sicherheit und Wirksamkeit getestet. Diese Medikamente sind nicht nur nicht getestet oder nicht registriert, sondern auch knapp.
Angesichts des großen Leidens und der hohen Sterblichkeitsraten ist es fair zu fragen, ob nicht registrierte und nicht getestete Medikamente besser sind als gar keine. Sollten solche Medikamente abgegeben werden und wenn ja, wer sollte sie angesichts ihrer äußerst begrenzten Versorgung erhalten? Ist es ethisch, nicht getestete Medikamente bei Patienten mit Ebola zu behandeln?, Ist es andererseits ethisch vertretbar, potenziell lebensrettende Medikamente sterbenden Patienten vorzuenthalten? Oder sollten die Medikamente vielleicht Gesundheitsdienstleistern vorbehalten sein, die daran arbeiten, die Krankheit einzudämmen?
Im August 2014 wurden zwei infizierte US-Helfer und ein spanischer Priester mit ZMapp behandelt, einem nicht registrierten Medikament, das an Affen, aber nicht an Menschen getestet worden war. Die beiden amerikanischen Helfer erholten sich, aber der Priester starb. Später in diesem Monat veröffentlichte die WHO einen Bericht über die Ethik der Behandlung von Patienten mit dem Medikament., Da Ebola oft tödlich ist, argumentierte das Gremium, dass es ethisch ist, die nicht registrierten Drogen zu geben, und unethisch, sie aus Sicherheitsgründen zurückzuhalten. Diese Situation ist ein Beispiel für den „mitfühlenden Einsatz“ außerhalb des etablierten Systems der Regulierung und Steuerung von Therapien.
Ebola in den USA
Am 24.September 2014 kam Thomas Eric Duncan im Texas Health Presbyterian Hospital in Dallas an und klagte über Fieber, Kopfschmerzen, Erbrechen und Durchfall—Symptome, die häufig bei Patienten mit Erkältung oder Grippe beobachtet werden., Nach der Untersuchung diagnostizierte ein Notarzt eine Sinusitis, verschrieb Antibiotika und schickte ihn nach Hause. Zwei Tage später kehrte Duncan mit einem Krankenwagen ins Krankenhaus zurück. Sein Zustand hatte sich verschlechtert und zusätzliche Blutuntersuchungen bestätigten, dass er mit dem Ebola-Virus infiziert war.
Weitere Untersuchungen ergaben, dass Duncan gerade aus Liberia zurückgekehrt war, einem der Länder inmitten einer schweren Ebola-Epidemie., September, neun Tage bevor er im Krankenhaus in Dallas auftauchte, hatte Duncan geholfen, einen von Ebola betroffenen Nachbarn in ein Krankenhaus in Liberia zu transportieren. Das Krankenhaus behandelte Duncan weiterhin, starb jedoch einige Tage nach seiner Aufnahme.

Abbildung 9. Forscher, die mit dem Ebola-Virus arbeiten, verwenden Schutzschichten gegen versehentliche Infektionen, einschließlich Schutzkleidung, Atmungssysteme und negative Luftdruckschränke für Bankarbeiten. (kredit: Änderung der Arbeit von Randal J., Schoepp)
Die Zeitleiste des Falls Duncan weist auf den Lebenszyklus des Ebola-Virus hin. Die Inkubationszeit für Ebola reicht von 2 Tagen bis 21 Tagen. Zwischen Duncans Exposition gegenüber der Virusinfektion und dem Auftreten seiner Symptome vergingen neun Tage. Dies entspricht zum Teil der Sonnenfinsternis im Wachstum der Viruspopulation. Während der Sonnenfinsternis wäre Duncan nicht in der Lage gewesen, die Krankheit auf andere zu übertragen. Sobald jedoch eine infizierte Person Symptome zeigt, wird die Krankheit sehr ansteckend., Das Ebola-Virus wird durch direkten Kontakt mit Körperflüssigkeitstropfen wie Speichel, Blut und Erbrochenem übertragen. Duncan könnte die Krankheit möglicherweise jederzeit auf andere übertragen haben, nachdem er Symptome hatte, vermutlich einige Zeit vor seiner Ankunft im Krankenhaus in Dallas. Sobald ein Krankenhaus erkennt, dass ein Patient wie Duncan mit dem Ebola-Virus infiziert ist, wird der Patient sofort unter Quarantäne gestellt, und Beamte des öffentlichen Gesundheitswesens initiieren eine Rückverfolgung, um alle zu identifizieren, mit denen ein Patient wie Duncan während des Zeitraums interagiert haben könnte, in dem er Symptome zeigte.,
Beamte des öffentlichen Gesundheitswesens konnten 10 Personen mit hohem Risiko (Familienmitglieder von Duncan) und 50 Personen mit niedrigem Risiko aufspüren, um sie auf Anzeichen einer Infektion zu überwachen. Keiner erkrankte an der Krankheit. Eine der Krankenschwestern, die mit Duncans Pflege beauftragt waren, infizierte sich jedoch. Dies machte zusammen mit Duncans anfänglicher Fehldiagnose deutlich, dass US-Krankenhäuser zusätzliches Training für medizinisches Personal bereitstellen mussten, um einen möglichen Ebola-Ausbruch in den USA zu verhindern.
- Welche Arten von Schulungen können Angehörige der Gesundheitsberufe darauf vorbereiten, aufkommende Epidemien wie den Ebola-Ausbruch von 2014 einzudämmen?,
- Was ist der Unterschied zwischen einem ansteckenden Erreger und einem infektiösen Erreger?
Schlüsselkonzepte und Zusammenfassung
- Viele Viren zielen auf bestimmte Wirte oder Gewebe ab. Einige können mehr als einen Host haben.
- Viele Viren folgen mehreren Stadien, um Wirtszellen zu infizieren. Diese Stadien umfassen Anheftung, Penetration, Überhitzung, Biosynthese, Reifung und Freisetzung.
- Bakteriophagen haben einen lytischen oder lysogenen Zyklus. Der lytische Zyklus führt zum Tod des Wirts, während der lysogene Zyklus zur Integration von Phagen in das Wirtsgenom führt.,
- Bakteriophagen injizieren DNA in die Wirtszelle, während tierische Viren durch Endozytose oder Membranfusion eindringen.
- Tierische Viren können Latenz erfahren, ähnlich wie Lysogenie für einen Bakteriophagen.
- Die Mehrheit der Pflanzenviren ist ssRNA mit positivem Strang und kann, wie bei Tierviren beobachtet, einer latenten, chronischen oder lytischen Infektion unterzogen werden.
- Die Wachstumskurve von Bakteriophagen-Populationen ist eine einstufige Multiplikationskurve und keine sigmoidale Kurve im Vergleich zur Bakterienwachstumskurve.,
- Bakteriophagen übertragen genetische Informationen zwischen Wirten entweder durch generalisierte oder spezialisierte Transduktion.
Multiple-Choice
Welche der folgenden führt zur Zerstörung der Wirtszellen?
- lysogener Zyklus
- lytischer Zyklus
- prophage
- gemäßigter Phage
In welcher der folgenden Phasen erhält ein Virus seine Hülle?,
- Befestigung
- penetration
- Montage
- release
Welche der folgenden Komponenten wird durch HIV in eine Zelle gebracht?
- eine DNA-abhängige DNA-Polymerase
- RNA-Polymerase
- Ribosom
- Reverse-Transkriptase
Ein Positiv-Strang-RNA-Virus:
- muss zuerst in eine mRNA konvertiert werden, bevor es übersetzt werden kann.
- kann direkt verwendet werden, um virale Proteine zu übersetzen.
- wird durch Wirtsenzyme abgebaut.
- wird von Wirtsribosomen nicht erkannt.
Wie lautet der Name für die Übertragung genetischer Informationen von einem Bakterium auf ein anderes Bakterium durch einen Phagen?,
- Transduktion
- Penetration
- Exzision
- translation
Denken Sie darüber nach
- Erklären Sie kurz den Unterschied zwischen dem Eintrittsmechanismus eines T-Virus-Bakteriophagen und eines tierischen Virus.
- Diskutieren Sie den Unterschied zwischen generalisierter und spezialisierter Transduktion.,
- Unterscheiden Sie zwischen lytischen und lysogenen Zyklen.
- Bakteriophagen haben lytische und lysogene Zyklen. Besprechen Sie die Vor-und Nachteile für die Phage.
- Wie hilft reverse Transkriptase einem Retrovirus bei der Entstehung einer chronischen Infektion?
- Diskutieren Sie einige Methoden, mit denen Pflanzenviren von einer erkrankten Pflanze auf eine gesunde übertragen werden.
- Beschriften Sie die fünf Stadien einer Bakteriophagen-Infektion in der Abbildung:
