Ikke alle Kollisjoner er Lik
For en gass ved romtemperatur og normale atmosfæriske trykket, det er om 1033 kollisjoner i hver eneste centimeter av plass hvert sekund. Hvis hver kollisjon mellom to reaktant molekyler gav produkter, som alle reaksjoner ville være komplett i en brøkdel av et sekund. For eksempel, når to billiard baller kolliderer, de bare sprette ut av hverandre., Dette er den mest sannsynlige utfallet hvis reaksjonen mellom A og B krever en betydelig forstyrrelse eller omorganisering av bindinger mellom atomene. For effektivt å kunne starte en reaksjon, kollisjoner må være tilstrekkelig energisk (eller har nok kinetisk energi) for å få til dette bond avbrudd. Dette er nærmere omtalt nedenfor.
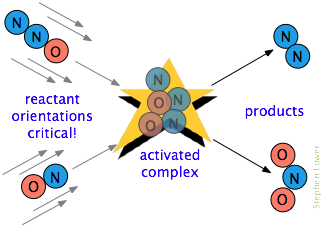
Det er ofte en ytterligere krav. I mange reaksjoner, spesielt de som involverer mer komplekse molekyler, reagerer arter må være innrettet på en måte som er hensiktsmessig for den aktuelle prosessen., For eksempel, i gass-fase reaksjon av dinitrogen oksid med nitrogenoksid, oksygen slutten av N2O må treffe nitrogen slutten av INGEN; å endre retning av enten molekylet hindrer reaksjon. På grunn av den omfattende randomisering av molekylære bevegelser i en gass eller væske, det er alltid nok riktig-orientert molekyler for noen av molekyler til å reagere. Imidlertid mer kritiske dette orientational kravet er, jo færre kollisjoner vil være effektiv.,
Energisk kollisjoner mellom molekyler føre interatomic obligasjoner til å strekke og bøye midlertidig svekkelse dem slik at de blir mer utsatt for spalting. Forvrengning av obligasjoner kan avsløre deres tilknyttede electron skyer interaksjoner med andre reaktanter som kan føre til dannelse av nye obligasjoner.,
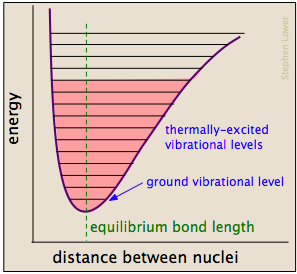
Kjemiske forbindelser har noen av egenskapene til mekanisk kilder: deres potensielle energi avhenge av i hvilken grad de er strukket eller komprimert. Hvert atom til atom bond kan beskrives ved en potensiell energi diagram som viser hvordan energien sin endringer med sin lengde., Når bond absorberer energi (enten fra oppvarming eller gjennom en kollisjon), det er hevet til et høyere quantized vibrasjons state (angitt med horisontale linjer) som svekker bindingen som sin lengde svinger mellom den utvidede grenser tilsvarende kurve.
En bestemt kollisjon vil vanligvis opphisse en rekke obligasjoner på denne måten. I løpet av 10-13 sekunder, denne eksitasjon er fordelt på de andre obligasjoner i molekylet i komplekse og uforutsigbare måter som kan konsentrere deg ekstra energi på en særlig sårbare punkt., De berørte bond kan strekke og bøye lenger, noe som gjør den mer utsatt for spalting. Selv om bindingen brytes ikke ved ren strekker seg, kan det bli forvrengt eller vridd, slik som å utsette nærheten electron skyer interaksjoner med andre reaktanter som kan gi en reaksjon.