Nu toate Ciocnirile sunt Egale
Pentru un gaz la temperatura camerei și presiune atmosferică normală, există aproximativ 1033 coliziuni în fiecare centimetru cub de spațiu în fiecare secundă. Dacă fiecare coliziune dintre două molecule reactante ar produce produse, toate reacțiile ar fi complete într-o fracțiune de secundă. De exemplu, atunci când două bile de biliard se ciocnesc, pur și simplu sări unul de celălalt., Acesta este cel mai probabil rezultat dacă reacția dintre A și B necesită o întrerupere sau rearanjare semnificativă a legăturilor dintre atomii lor. Pentru a iniția efectiv o reacție, coliziunile trebuie să fie suficient de energice (sau să aibă suficientă energie cinetică) pentru a produce această întrerupere a legăturii. Acest lucru este discutat mai jos.
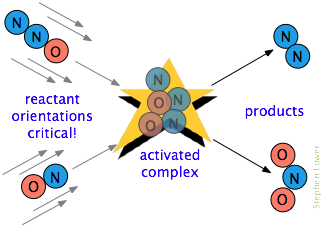
există adesea o cerință suplimentară. În multe reacții, în special cele care implică molecule mai complexe, speciile care reacționează trebuie să fie orientate într-o manieră adecvată procesului particular., De exemplu, în reacția în fază gazoasă a oxidului de azot cu oxid nitric, capătul de oxigen al N2O trebuie să atingă capătul de azot al NO; modificarea orientării fiecărei molecule împiedică reacția. Datorită randomizării extinse a mișcărilor moleculare într-un gaz sau lichid, există întotdeauna suficiente molecule orientate corect pentru ca unele dintre molecule să reacționeze. Cu toate acestea, cu cât această cerință orientativă este mai critică, cu atât mai puține coliziuni vor fi eficiente.,coliziunile energetice dintre molecule determină întinderea și îndoirea legăturilor interatomice, slăbindu-le temporar, astfel încât acestea să devină mai sensibile la scindare. Distorsiunea legăturilor poate expune norii de electroni asociați la interacțiuni cu alți reactanți care ar putea duce la formarea de noi legături.,
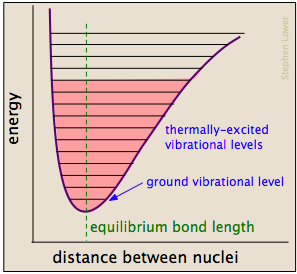
legături Chimice au unele dintre proprietățile mecanice izvoare: potențialul lor energii depinde de măsura în care acestea sunt întinse sau comprimate. Fiecare legătură atom-atom poate fi descrisă printr-o diagramă energetică potențială care arată modul în care energia sa se schimbă cu lungimea sa., Când legătura absoarbe energia (fie din încălzire, fie printr-o coliziune), este ridicată la o stare vibrațională cuantificată mai mare (indicată de liniile orizontale) care slăbește legătura, deoarece lungimea ei oscilează între limitele extinse corespunzătoare curbei.
o anumită coliziune va excita de obicei un număr de legături în acest fel. În aproximativ 10-13 secunde, această excitație este distribuită între celelalte legături din moleculă în moduri complexe și imprevizibile care pot concentra energia adăugată într-un punct deosebit de vulnerabil., Legătura afectată se poate întinde și se poate îndoi mai departe, făcând-o mai susceptibilă la scindare. Chiar dacă legătura nu se rupe prin întindere pură, ea poate deveni distorsionată sau răsucită, astfel încât să expună norii de electroni din apropiere la interacțiuni cu alți reactanți care ar putea încuraja o reacție.