elementul chimic aluminiu este clasificat ca un alt metal. A fost descoperit în anii 1750 de Andreas Marggraf.,

Data Zone
| Classification: | Aluminum is an ‘other metal’ |
| Color: | silvery |
| Atomic weight: | 26.98154 g/mol |
| State: | solid |
| Melting point: | 660.32 oC, 933.57 K |
| Boiling point: | 2466.85 oC, 2740.,00 K |
| Electrons: | 13 |
| Protons: | 13 |
| Neutrons in most abundant isotope: | 14 |
| Electron shells: | 2,8,3 |
| Electron configuration: | 1s2 2s2 2p6 3s2 3p1 |
| Density @ 20oC: | 2.702 g/cm3 |
Show more, including: Heats, Energies, Oxidation,
Reactions, Compounds, Radii, Conductivities
| Atomic volume: | 9.,98 cm3/mol | ||
| Structure: | fcc: face-centered cubic | ||
| Hardness: | 2.8 mohs | ||
| Specific heat capacity | 0.90 J g-1 K-1 | ||
| Heat of fusion | 10.790 kJ mol-1 | ||
| Heat of atomization | 326 kJ mol-1 | ||
| Heat of vaporization | 293.40 kJ mol-1 | ||
| 1st ionization energy | 577.6 kJ mol-1 | ||
| 2nd ionization energy | 1816.6 kJ mol-1 | ||
| 3rd ionization energy | 2744.,7 kJ mol-1 | ||
| Electron affinity | 42.6 kJ mol-1 | ||
| Minimum oxidation number | 0 | ||
| Min. common oxidation no. | 0 | ||
| Maximum oxidation number | 3 | ||
| Max. common oxidation no. | 3 | ||
| Electronegativity (Pauling Scale) | 1.61 | ||
| Polarizability volume | 8.,> | Reaction with 15 M HNO3 | passivated |
| Reaction with 6 M HCl | mild, ⇒ H2, AlCl3 | ||
| Reaction with 6 M NaOH | mild, ⇒ H2, – | ||
| Oxide(s) | Al2O3 | ||
| Hydride(s) | AlH3 | ||
| Chloride(s) | AlCl3 & Al2Cl6 | ||
| Atomic radius | 125 pm | ||
| Ionic radius (1+ ion) | – | ||
| Ionic radius (2+ ion) | – | ||
| Ionic radius (3+ ion) | 53.,5 pm | ||
| Ionic radius (1- ion) | – | ||
| Ionic radius (2- ion) | – | ||
| Ionic radius (3- ion) | – | ||
| Thermal conductivity | 237 W m-1 K-1 | ||
| Electrical conductivity | 37.6676 x 106 S m-1 | ||
| Freezing/Melting point: | 660.32 oC, 933.,57 K |
Louis de Morveau crezut un nou metal ar putea fi descoperite în oxid de alumină. Avea dreptate, dar nu a reușit să-l izoleze. De Morveau a conceput prima metodă sistematică de denumire a substanțelor chimice și, după cum putem vedea, a fost un pionier al baloniștilor.,
Aluminum’s Periodic Table
Neighborhood
| Group 2 or 12 |
Group 13 |
Group 14 |
|
| 2 | 4 Be |
5 B |
6 C |
| 3 | 12 Mg |
13 Al |
14 Si |
| 4 | 30 Zn |
31 Ga |
32 Ge |
Discovery of Aluminum
oamenii au folosit alum din cele mai vechi timpuri pentru vopsire, bronzare și pentru a opri sângerarea. Alum este sulfat de aluminiu de potasiu.în anii 1750, chimistul german Andreas Marggraf a descoperit că poate folosi o soluție alcalină pentru a precipita o nouă substanță din alum. Marggraf a fost anterior prima persoană care a izolat zincul în 1746.substanța Marggraf obținută din alum a fost numită alumină de chimistul francez Louis de Morveau în 1760. Acum știm că alumina este oxid de aluminiu – formula chimică Al2O3.,De Morveau credea că alumina conține un nou element metalic, dar, la fel ca Marggraf, nu a putut extrage acest metal din oxidul său. (1), (2)
în 1807 sau 1808, chimistul englez Humphry Davy a descompus alumina într-un arc electric pentru a obține un metal. Metalul nu era aluminiu pur, ci un aliaj de aluminiu și fier.Davy a numit noul alumiu metalic, apoi l-a redenumit aluminiu. (3)
aluminiul a fost izolat pentru prima dată în 1825 de Hans Christian Ørsted (Oersted) din Copenhaga, Danemarca, care a raportat: „o bucată de metal care, în culoare și luciu, seamănă oarecum cu staniu.,Ørsted a produs Aluminiu prin reducerea clorurii de aluminiu folosind un amalgam de potasiu-mercur. Mercurul a fost îndepărtat prin încălzire pentru a lăsa aluminiu.
chimistul German Friedrich Wöhler (Woehler) repetat experimentul lui Ørsted, dar a găsit-o dat numai de potasiu metalic. Wöhler a dezvoltat metoda în continuare doi ani mai târziu, reacționând triclorura de aluminiu volatalizată cu potasiu pentru a produce cantități mici de aluminiu. (1)
în 1856 Berzelius a declarat că Wöhler a fost cel care a reușit în 1827. Prin urmare, lui Wöhler i se acordă de obicei credit pentru descoperire., mai recent, Fogh a repetat experimentele originale și a arătat că metoda lui Ørsted poate da rezultate satisfăcătoare. acest lucru a consolidat prioritatea lucrării originale a lui Ørsted și poziția sa de descoperitor al aluminiului. Timp de aproape trei decenii, aluminiul a rămas o noutate, scump de produs și mai valoros decât aurul, până când în 1854 Henri Saint-Claire Deville din Paris, Franța a găsit o modalitate de a înlocui potasiul cu sodiu mult mai ieftin în reacția de izolare a aluminiului., Aluminiu a devenit apoi mai popular, dar, pentru că era încă destul de scump, a fost folosit în situații Ornamentale, mai degrabă decât practice.
în cele din Urmă, în anul 1886, chimistul American Charles Martin Hall și chimistul francez Paul Héroult independent inventat Sala-Héroult proces, care ieftin izolate de aluminiu de metal din oxid electrolitic.
aluminiul este încă fabricat folosind procesul Hall-Héroult astăzi.
fapte interesante despre Aluminiu
- fabricarea aluminiului necesită multă energie – 17.,4 megawatt ore de energie electrică pentru a produce o tonă metrică de aluminiu; adică de trei ori mai multă energie decât este necesară pentru a produce o tonă metrică de oțel. (5)
- aluminiul este un metal excelent de reciclat. Reciclarea folosește doar 5% din energia necesară pentru a produce aluminiu din minereul său, bauxita. (6)
- aluminiu nu se lipește de magneți în condiții normale.
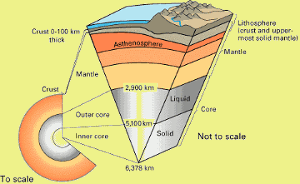
- există mai mult aluminiu în scoarța Pământului decât orice alt metal. La aproximativ 8%, aluminiul este al treilea element cel mai abundent din crusta planetei noastre, în spatele oxigenului și siliciului.,
- în ciuda abundenței sale ridicate, în anii 1850 aluminiul era mai valoros decât aurul. În 1852, aluminiul avea un preț de 1200 USD pe kg, iar aurul era de 664 USD pe kg.
- prețurile aluminiului ilustrează pericolele speculațiilor financiare: în 1854, Saint-Claire Deville a găsit o modalitate de a înlocui potasiul cu sodiu mult mai ieftin în reacția de izolare a aluminiului. Până în 1859, aluminiul avea un preț de 37 USD pe kg; prețul său a scăzut cu 97% în doar cinci ani.,
- unde articolul anterior evidențiază pericolele speculațiilor, acest articol evidențiază unul dintre triumfurile chimiei: procesul electrolitic Hall-Heroult a fost descoperit în 1886. Până în 1895, prețul aluminiului a scăzut la doar 1, 20 USD pe kg.
- Ruby geme sunt în principal oxid de aluminiu în care un număr mic de ioni de aluminiu au fost înlocuiți cu ioni de crom.
- aluminiul este fabricat în focurile nucleare ale stelelor grele atunci când un proton adaugă magneziu. (Magneziul este el însuși produs în stele prin fuziunea nucleară a doi atomi de carbon.,) (7)


aspect și caracteristici
efecte dăunătoare:
nu există probleme dovedite; ingestia poate provoca boala alzheimer
caracteristici:
aluminiul este un metal alb-argintiu., Nu se lipește de magneți (este paramagnetic și astfel magnetismul său în condiții normale este foarte, foarte slab). Este un conductor electric excelent. Este de densitate scăzută și ductilitate ridicată. Este prea reactiv pentru a fi frecvent găsit ca metal deși, foarte rar, metalul nativ poate fi găsit. (8)
aspectul aluminiului este dărâmat și reactivitatea acestuia este pasivată de o peliculă de oxid de aluminiu care se formează în mod natural pe suprafața metalului în condiții normale. Filmul de oxid are ca rezultat un material care rezistă la coroziune., Filmul poate fi îngroșat folosind electroliză sau agenți de oxidare, iar aluminiul în această formă va rezista atacului acizilor diluați, alcalinelor diluate și acidului azotic concentrat.aluminiul se află suficient de departe în partea dreaptă a tabelului periodic încât arată unele indicii de comportament nemetalic, reacționând cu alcalii fierbinți pentru a forma ioni de aluminat – precum și reacția metalică mai tipică cu acizii pentru a elibera gazul de hidrogen și a forma ionul metalic încărcat pozitiv, Al3+. adică aluminiul este amfoteric.aluminiu pur este destul de moale și lipsit de rezistență., Aluminiul utilizat în aplicații comerciale are cantități mici de siliciu și fier (mai puțin de 1%) adăugate, rezultând o rezistență și o duritate mult îmbunătățite.ca urmare a densității sale scăzute, a costurilor reduse și a rezistenței la coroziune, aluminiul este utilizat pe scară largă în întreaga lume. este utilizat într-o gamă largă de produse, de la cutii de băuturi la rame de ferestre și bărci la aeronave. Un Boeing 747-400 conține 147.000 de lire sterline (66.150 kg) de aluminiu de înaltă rezistență.spre deosebire de unele metale, aluminiul nu are aromă – de unde și utilizarea sa pe scară largă în ambalajele alimentare și vasele de gătit.,deși nu este la fel de bun ca argintul sau cuprul, aluminiul este un conductor electric excelent. De asemenea, este considerabil mai ieftin și mai ușor decât aceste metale, deci este utilizat pe scară largă în liniile electrice aeriene.dintre Toate metalele, numai fierul este utilizat mai mult decât aluminiul.abundența scoarței terestre: 8,23% în greutate, 6,32% în moli
abundența sistemului solar: 56 ppm în Greutate, 2,7 ppm în moli
Cost, pur: $15,72 per 100g
Cost, vrac: $0.,20 la 100g
Sursa: aluminiul este cel mai abundent metal din scoarța terestră și al treilea cel mai mare element din scoarța terestră, după oxigen și siliciu. Aluminiu este prea reactiv pentru a fi găsit pur. Bauxita (în principal oxid de aluminiu) este cel mai important minereu.
izotopi: 15 ale căror timpi de înjumătățire sunt cunoscuți, numerele de masă de la 22 la 35. Dintre acestea, doar două apar în mod natural: 27Al, care este stabilă, și 26Al, care este radioactive cu timp de înjumătățire este 7.17 x 105 ani. 26al este format prin bombardarea cu raze cosmice a argonului în atmosfera Pământului.,

Cite această Pagină
Pentru on-line de legătură, vă rugăm să copiați și inserați codul în una din următoarele:
<a href="https://www.chemicool.com/elements/aluminum.html">Aluminum</a>
sau
<a href="https://www.chemicool.com/elements/aluminum.html">Aluminum Element Facts</a>
Pentru a cita această pagină într-un mediu academic document, vă rugăm să folosiți următoarele MLA conforme citare:
"Aluminum." Chemicool Periodic Table. Chemicool.com. 26 Jul. 2014. Web. <https://www.chemicool.com/elements/aluminum.html>.