alkuaine alumiini on luokiteltu muut-metallia. Sen löysi 1750-luvulla Andreas Marggraf.,

Data Zone
| Classification: | Aluminum is an ‘other metal’ |
| Color: | silvery |
| Atomic weight: | 26.98154 g/mol |
| State: | solid |
| Melting point: | 660.32 oC, 933.57 K |
| Boiling point: | 2466.85 oC, 2740.,00 K |
| Electrons: | 13 |
| Protons: | 13 |
| Neutrons in most abundant isotope: | 14 |
| Electron shells: | 2,8,3 |
| Electron configuration: | 1s2 2s2 2p6 3s2 3p1 |
| Density @ 20oC: | 2.702 g/cm3 |
Show more, including: Heats, Energies, Oxidation,
Reactions, Compounds, Radii, Conductivities
| Atomic volume: | 9.,98 cm3/mol | ||
| Structure: | fcc: face-centered cubic | ||
| Hardness: | 2.8 mohs | ||
| Specific heat capacity | 0.90 J g-1 K-1 | ||
| Heat of fusion | 10.790 kJ mol-1 | ||
| Heat of atomization | 326 kJ mol-1 | ||
| Heat of vaporization | 293.40 kJ mol-1 | ||
| 1st ionization energy | 577.6 kJ mol-1 | ||
| 2nd ionization energy | 1816.6 kJ mol-1 | ||
| 3rd ionization energy | 2744.,7 kJ mol-1 | ||
| Electron affinity | 42.6 kJ mol-1 | ||
| Minimum oxidation number | 0 | ||
| Min. common oxidation no. | 0 | ||
| Maximum oxidation number | 3 | ||
| Max. common oxidation no. | 3 | ||
| Electronegativity (Pauling Scale) | 1.61 | ||
| Polarizability volume | 8.,> | Reaction with 15 M HNO3 | passivated |
| Reaction with 6 M HCl | mild, ⇒ H2, AlCl3 | ||
| Reaction with 6 M NaOH | mild, ⇒ H2, – | ||
| Oxide(s) | Al2O3 | ||
| Hydride(s) | AlH3 | ||
| Chloride(s) | AlCl3 & Al2Cl6 | ||
| Atomic radius | 125 pm | ||
| Ionic radius (1+ ion) | – | ||
| Ionic radius (2+ ion) | – | ||
| Ionic radius (3+ ion) | 53.,5 pm | ||
| Ionic radius (1- ion) | – | ||
| Ionic radius (2- ion) | – | ||
| Ionic radius (3- ion) | – | ||
| Thermal conductivity | 237 W m-1 K-1 | ||
| Electrical conductivity | 37.6676 x 106 S m-1 | ||
| Freezing/Melting point: | 660.32 oC, 933.,57 K |
Louis de Morveau uskoi uuden metal voisi olla löydettiin alumiinioksidin oksidi. Hän oli oikeassa, mutta ei pystynyt eristämään sitä. De Morveau kehitti ensimmäisen systemaattisen menetelmän kemikaalien nimeämiseksi, ja kuten näemme, hän oli edelläkävijä balloonistina.,
Aluminum’s Periodic Table
Neighborhood
| Group 2 or 12 |
Group 13 |
Group 14 |
|
| 2 | 4 Be |
5 B |
6 C |
| 3 | 12 Mg |
13 Al |
14 Si |
| 4 | 30 Zn |
31 Ga |
32 Ge |
Discovery of Aluminum
ihmiset ovat käyttäneet alumia muinaisista ajoista lähtien värjäykseen, rusketukseen ja verenvuodon tyrehdyttämiseen. Alum on kaliumalumiinisulfaattia.
Vuonna 1750-luvulla saksalainen kemisti Andreas Marggraf löysi hän voisi käyttää alkali ratkaisu sakka uuden aineen aluna. Margraf oli aiemmin eristänyt sinkin ensimmäisenä vuonna 1746.
aineen Marggraf saatu aluna oli nimeltään alumiinioksidin ranskalainen kemisti Louis de Morveau vuonna 1760. Tiedämme nyt, että alumiinioksidi on alumiinioksidi-kemiallinen kaava Al2O3.,
De Morveau uskoi, alumiinioksidin sisälsi uuden metallinen elementti, mutta, kuten Marggraf, hän ei voinut poimia tämä metalli on sen oksidi. (1), (2)
Vuonna 1807 tai 1808, englanti kemisti Humphry Davy hajonnut alumiinioksidin valokaaren saada metallia. Metalli ei ollut puhdasta alumiinia, vaan alumiinin ja raudan seosta.
Davy kutsui uutta metallioksidia, jonka jälkeen se nimettiin uudelleen alumiiniksi. (3)
Alumiini oli ensin eristetty vuonna 1825 Hans Christian Ørsted (Oersted) Kööpenhaminassa, Tanskassa, joka ilmoitti, ”pala metallia, joka väri ja kiilto hieman muistuttaa tinaa.,”
Ørsted valmisti alumiinia pelkistämällä alumiinikloridia kalium-elohopea-amalgaamin avulla. Elohopea poistettiin kuumentamalla alumiinista.
saksalainen kemisti Friedrich Wöhler (Woehler) toistuva Ørsted on kokeilu, mutta se tuotti vain kaliumia metallia. Wöhler kehitti menetelmän vielä kaksi vuotta myöhemmin reagoiden volatalisoituneeseen alumiinitrikloridiin kaliumin kanssa tuottamaan pieniä määriä alumiinia. (1)
vuonna 1856 Berzelius totesi wöhlerin onnistuneen vuonna 1827. Wöhler saa siis yleensä kunnian löydöstä.,
viime aikoina, Fogh toisti alkuperäisen kokeiluja ja osoitti, että Ørsted menetelmä voi antaa tyydyttäviä tuloksia.
Tämä on vahvistanut prioriteetti Ørsted on alkuperäinen työ, ja hänen asemaansa löytäjä alumiini. (4)
lähes kolme vuosikymmentä, alumiini pysyi uutuus, kallista tuottaa ja arvokkaampaa kuin kulta, kunnes vuonna 1854 Henri Saint-Claire Deville Pariisissa, Ranskassa keinon korvata kalium paljon halvempaa natriumin reaktio eristää alumiini., Alumiini sitten tuli suosittu, mutta koska se oli vielä varsin kallista, käytettiin koriste pikemminkin kuin käytännön tilanteissa.
Lopulta, vuonna 1886 Amerikkalainen kemisti Charles Martin Hall ja ranskalainen kemisti Paul Héroult itsenäisesti keksi Hall-Héroult prosessi, joka edullisesti eristää alumiini metalli sen oksidi elektrolyyttisesti.
alumiinia valmistetaan vielä nykyäänkin Hall-Héroult-prosessilla.
Mielenkiintoisia Faktoja Alumiini
- Alumiinin valmistus vie paljon energiaa – 17.,4 megawattituntia sähköenergiaa yhden metrisen tonnin alumiinia tuottamiseksi; se on kolme kertaa enemmän energiaa kuin tarvitaan metrisen tonnin terästä. (5)
- Alumiini on suuri metalli kierrättää. Kierrätys käyttää vain 5 prosenttia siitä energiasta, jota tarvitaan alumiinin tuottamiseen sen malmista, bauksiitista. (6)
- alumiini ei tartu magneetteihin normaaliolosuhteissa.
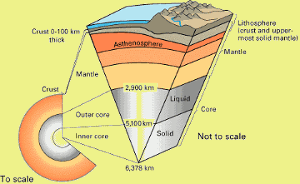
- maankuoressa on enemmän alumiinia kuin missään muussa metallissa. Noin 8 prosentin kohdalla alumiini on maapallon kuoren kolmanneksi runsain alkuaine hapen ja piin takana.,
- suuresta runsaudestaan huolimatta 1850-luvulla alumiini oli kultaa arvokkaampaa. Vuonna 1852 alumiinin hinnaksi tuli 1 200 dollaria kilolta ja kullaksi 664 dollaria kilolta.
- Alumiinin hinnat kuvaavat vaarat taloudellinen keinottelu: vuonna 1854 Saint-Claire Deville keinon korvata kalium paljon halvempaa natriumin reaktio eristää alumiini. Vuoteen 1859 mennessä alumiinin hinnaksi tuli 37 dollaria kilolta; sen hinta oli laskenut vain viidessä vuodessa 97 prosenttia.,
- Mihin edellinen erä korostaa vaarojen spekulointia, tämä tuote kohokohtia yksi voittaa kemia: Hall-Heroult elektrolyyttinen prosessi, löydettiin vuonna 1886. Vuoteen 1895 mennessä alumiinin hinta oli pudonnut vain 1,20 dollariin kilolta.
- Rubiiniset jalokivet ovat pääasiassa alumiinioksidia, jossa pieni osa alumiini-ioneista on korvattu Kromi-ioneilla.
- alumiinia tehdään raskaiden tähtien ydinpaloissa, kun protoni lisää magnesiumia. (Magnesium on itse tehty tähdissä kahden karbonin ydinfuusiolla.,) (7)


Ulkoasu ja Ominaisuudet
Haitallisia vaikutuksia:
Ole todistettu kysymyksiä; nieleminen voi aiheuttaa alzheimerin tauti
Ominaisuudet:
Alumiini on hopeanhohtoinen valkoinen metalli., Se ei tartu magneetteihin (se on paramagneettinen ja niin sen magnetismi normaaliolosuhteissa on hyvin, hyvin heikko). Se on erinomainen sähköjohdin. Se on alhainen tiheys ja suuri sitkeys. Se on liian reaktiivinen löydettäväksi yleisesti metallina, vaikka hyvin harvoin sitä löytyy. (8)
Alumiini ulkonäkö on dulled ja sen reaktiivisuus on passivoitu, jonka elokuva alumiini-oksidi, joka luonnollisesti muodostaa pinnalle metalli normaaleissa olosuhteissa. Oksidikalvo johtaa materiaaliin, joka kestää korroosiota., Elokuva voi olla paksuuntunut käyttäen elektrolyysin tai hapettavat aineet ja alumiini tässä muodossa vastustaa hyökkäys laimentaa happoja, laimeita emäksiä ja väkevää typpihappoa.
Alumiini sijaitsee riittävän kaukana oikealla puolella jaksollisen, että se osoittaa joitakin vinkkejä epämetalli käyttäytymistä, reagoi kuuma emäksiä muodostaa aluminate-ioneja – sekä enemmän tyypillinen metalli reaktio happojen kanssa vapauttaa vetykaasua ja muodostavat positiivisesti varautunut metalli-ioni, Al3+. eli alumiini on amfoteerista.
puhdas alumiini on melko pehmeää ja lujuudeltaan puutteellista., Alumiini käytetään kaupallisissa sovelluksissa on pieniä määriä piitä ja rautaa (alle 1%) lisätään, mikä suuresti parantaa lujuutta ja kovuutta.
alumiinin
käytön alhaisen tiheyden, edullisuuden ja korroosionkestävyyden vuoksi alumiinia käytetään laajalti ympäri maailmaa.
sitä käytetään monenlaisissa tuotteissa juomatölkeistä ikkunanpuitteisiin ja veneistä lentokoneisiin. Boeing 747-400 sisältää 147 000 paunaa (66 150 kg) lujaa alumiinia.
erona joihinkin metalleihin alumiinilla ei ole aromia, joten sitä käytetään laajalti elintarvikepakkauksissa ja ruukuissa.,
vaikka alumiini ei olekaan aivan yhtä hyvä kuin hopea tai kupari, se on erinomainen sähköjohdin. Se on myös huomattavasti halvempaa ja kevyempää kuin nämä metallit, joten sitä käytetään laajalti ilmajohtojen.
kaikista metalleista vain rautaa käytetään laajemmin kuin alumiinia.
Runsaasti ja Isotoopit
Runsaasti maankuoressa: 8.23 % painosta, 6.32 % myyrät
Runsaasti aurinkokunta: 56 ppm painosta, 2.7 ppm myyrät
Kustannukset, puhdas: $15.72 / 100 g
Hinta, bulk: $0.,20 per 100g
Lähde: Alumiini on yleisin metalli maankuoressa ja kolmanneksi yleisin alkuaine maankuoressa, hapen ja silikonin jälkeen. Alumiini on liian reaktiivista ollakseen puhdasta. Bauksiitti (pääasiassa alumiinioksidi) on tärkein Malmi.
isotoopit: 15 joiden puoliintumisajat tunnetaan, massaluvut 22-35. Näistä vain kaksi esiintyy luonnostaan: 27Al, joka on vakaa, ja 26Al, joka on radioaktiivisen puoli-elämä on 7.17 x 105 vuotta. 26al muodostuu kosmisen säteilyn pommittamasta argonista Maan ilmakehässä.,

Cite this Page
online yhdistää, kopioi ja liitä jokin seuraavista:
<a href="https://www.chemicool.com/elements/aluminum.html">Aluminum</a>
tai
<a href="https://www.chemicool.com/elements/aluminum.html">Aluminum Element Facts</a>
mainita tämän sivun akateeminen asiakirja, käytä seuraavaa MLA-yhteensopiva lainaus:
"Aluminum." Chemicool Periodic Table. Chemicool.com. 26 Jul. 2014. Web. <https://www.chemicool.com/elements/aluminum.html>.