rautaoksidi, jota kutsutaan myös sen IUPAC-nimi rauta-Trihydraatti tai rauta(III) oksidi, on epäorgaaninen yhdiste, jota edustaa kemiallinen kaava-Fe2O3 tai Fe2H6O3 . Se on yksi tärkeimmistä raudan oksideista, kaksi muuta ovat ferrosoferrinen oksidi (Fe3O4) ja rautaoksidi (FeO). Se esiintyy luontaisesti mineraalihematiittina .,
rautaoksidi Kaava
Sammutettua rautaoksidi
Se on punertava-ruskea hyytelömäinen yhdiste tuotetaan, kun emästä sisältävien liuosten Fe(III) suoloja. Sitä kutsutaan myös vesipitoista rautaoksidia, ja se voidaan kemiallisesti edustettuina joko Fe2O3.H2O tai Fe (O)OH . Jotkut yleisiä muotoja sammutettua rautaoksidia sisältävät punaista lepidocrocite, joka ilmenee ulkoisesti ruosteessa ja oranssi götiitti, joka tapahtuu sisällä ruosteessa.,
Miten on Rautaoksidia valmis
rautaoksidia on syntetisoitu laboratoriossa läpi elektrolyysin natriumbikarbonaattia ratkaisu, joka toimii inertti elektrolyytti, ja rauta-anodi. Elektrolyyttinen muuntaminen rautaa sammutettua rauta (III) oksidi on edustettuina:
4Fe + 3O2 + 2H2O → 4 FeO(OH)
sammutettua rauta (III) oksidi, näin tuotettu, tapahtuu kuivuminen noin 200 °C: ssa muodostaen rautaoksidia ., voit ferrosulfaatti (FeSO4), joka on edelleen hapettunut rauta sulfaatti :
- FeS2 + 7O+ H2O → FeSO4 + H2SO4
- 2FeSO4 + H2SO4 + O → Fe2(SO4)3 + H2O
Alumiini korvaa Rautaa rautaoksidi
Alumiini-ja rautaoksidi tehdään redox-reaktio, jossa metalli korvaa rauta muodostaa alumiinioksidi:
Fe2O3 + 2Al → Al2O3 + 2Fe
Ominaisuudet ja Ominaisuudet rautaoksidi
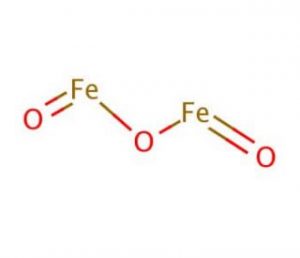
Rakenne rautaoksidi
Käyttää
- iron teollisuuden tuottaa teräs ja seokset .,
- Rauta-oksidi-jauhe, jota kutsutaan myös kultasepänliike rouge, käytetään kiillotus linssit ja metalli koruja .
- sen rakeista muotoa käytetään suodatusvälineenä fosfaattien vetämiseen suolaisen veden akvaarioissa .
- Kuten FDA-hyväksytty Pigmentti Ruskea 6 ja Pigment Red 101, käytettäväksi kosmetiikassa .
- biolääketieteen sovelluksissa, koska sen nanohiukkaset ovat myrkyttömiä ja biologisesti .
Onko se Vaarallista
Pitkäaikainen altistuminen sen savun tai pölyn seurauksena voi pneumokonioosi kuume, vilunväristykset, särky, hengenahdistus, ja yskä ., Toistuva kosketus silmiin voi värjätä sen ja aiheuttaa pysyvää rautavärjäystä .
- Rauta(III) oksidi – Chemspider.com
- Punainen rautaoksidi – Pubchem.ncbi.nlm.hih.gov
- Magnetiitti (Fe3O4) – Pubchem.ncbi.nlm.nih.gov
- Rauta-oksidi – Pubchem.ncbi.nlm.nih.gov
- FEI:50819 – rautaoksidi – Ebi.ac.uk
- rautaoksidi Pölyn ja Savun (kuten Fe) – Cdc.gov
- Kinetiikka ja mekanismi nestehukka γ-FeOOH – Researchgate.net
- Rauta(III) Oksidi Hiukkasia – Americanelements.com
- rautaoksidi – Chemicalbook.,com
- Magneettinen Materiaalien Ominaisuuksia – Sigmaaldrich.com
- Rauta(III) Oksidi – Chem.libretexts.org
- rautaoksidi (Fe2O3), Kaustinen (Yhdiste) – Pubchem.ncbi.nlm.nih.gov
- hapettumista ferrosulfaatti, jotta rauta sulfaatti avulla ilma – Archive.org
- Käyttää Rauta-Oksidi – Zjunited.com
- Vaarallinen Aine Fact Sheet rautaoksidi – Nj.gov