Inleiding
Adipose-derived stromale cellen (ASCs) zijn multipotent en immunoprivileged, waardoor ze ideale kandidaten zijn voor therapeutische doeleinden (Bourin et al., 2013; Ma et al., 2014; Kallmeyer and Pepper, 2015). ASC ‘ s kunnen worden geà soleerd met minimaal invasieve technieken uit verschillende vetweefsel depots in het lichaam (Zuk et al., 2001)., Ze worden gekenmerkt door hun vermogen om zich te hechten aan plastic, een uniek oppervlak marker profiel en de capaciteit om te differentiëren in bot, vet en kraakbeen (Dominici et al., 2006; Bourin et al., 2013). ASC ‘ s bestaan uit ~15-30% van de stromale vasculaire fractie (SVF) van vetweefsel (Bourin et al., 2013; Zuk, 2013), en moet ex vivo worden uitgebreid om voldoende celaantallen voor therapeutische doeleinden te verkrijgen.,
het verstrekken van veilige en gereguleerde celtherapieproducten aan patiënten vereist naleving van good manufacturing practices (GMP), en GMP-richtlijnen dienen te worden nageleefd gedurende het proces van isoleren, uitbreiden en differentiëren van ASC ‘ s (Giancola et al., 2012). De talrijke reagentia gebruikt om ASC ‘ s te isoleren en uit te breiden voor onderzoeksdoeleinden zijn van dierlijke oorsprong of zijn niet van klinische kwaliteit; daarom moeten deze worden vervangen door meer geschikte alternatieven volgens GMP-normen (Halme and Kessler, 2006; Riis et al., 2015)., We bekijken de keuze van serumsuppletie die kan worden gebruikt voor ASC-expansie in plaats van foetaal runderserum (FBS), en beschrijven hun effecten in vitro en in vivo zoals gerapporteerd in de literatuur.,
richtlijnen en technieken die worden gebruikt om de eigenschappen van Adipose afgeleide stromale cellen te beoordelen
de International Society of Cellular Therapy (ISCT) en de International Fat Applied Technology Society (IFATS) hebben een aantal minimale criteria en richtlijnen aanbevolen voor de karakterisering van ASCs (Dominici et al., 2006; Bourin et al., 2013)., Deze criteria omvatten het vermogen van de ASC ‘ s om zich te hechten aan kunststof, hun oppervlak marker profiel en hun trilineage differentiatie potentieel. De meest recente position paper beschrijft levensvatbaarheid en proliferatie als aanvullende metingen aan de oorspronkelijke karakterisatiecriteria. Verder zijn experimentele methoden en assays gedefinieerd om de karakterisatiecriteria te meten (Bourin et al., 2013)., Deze criteria zijn beïnvloed door tal van factoren zoals de liposuctie techniek, de SVF isolatie techniek en de media en suppletie gebruikt tijdens het uitbreidingsproces (Koellensperger et al., 2014; Bajek et al., 2015; Busser et al., 2015). Volgens de richtlijnen ISCT en IFATS, wordt het aanbevolen en aanvaarde onderzoekspraktijk om de naleving van de bovengenoemde richtlijnen voor elke isolatie en cultuurvoorwaarde te bevestigen om de resulterende celpopulatie als ASCs te classificeren.,
technieken en methoden die worden gebruikt om ASC ’s te karakteriseren
morfologie en therapietrouw
eenmaal gezaaid vertonen adherente ASC’ s een aparte morfologie, die kan worden beschreven als dun, langwerpig en spindelvormig. De morfologische beoordeling van ASC ‘ s wordt meestal voorgevormd met behulp van lichtmicroscopie (Trojahn Kølle et al., 2013).
proliferatie
de richtlijnen van ISCT en IFATS hebben aanbevolen dat de proliferatie en de frequentie van ACSS van voorlopercellen worden gemeten door middel van een fibroblastoïde colony-forming unit assay (Bourine et al., 2013)., Andere technieken die in de studies worden gebruikt die in dit overzicht worden aangehaald maken gebruik van het tellen van levensvatbare cellen of het meten van de proliferatieve capaciteit van ASCs gebruikend immunohistochemie. De telmethoden omvatten (1) het tellen van de cellen met behulp van een viability dye en een hemocytometer, (2) het tellen van de cellen met behulp van ofwel het tellen van parels of kleuring technieken en stroom cytometrische analyse, en (3) het gebruik van colorimetrische assays die levensvatbare cellen meten in een spectrofotometer (Gharibi and Hughes, 2012; Trojahn Kølle et al., 2013; Bogdanova et al., 2014; Atashi et al., 2015; Johal et al., 2015; Oikonomopoulos et al., 2015).,
Immunofenotype
De ISCT-en IFATS-richtlijnen hebben de expressie van meerdere oppervlaktemarkers en hun verwachte percentages als een vaste eis vermeld in hun positieverklaring. Ze hebben ook aanbevolen dat oppervlakte marker expressie moet worden gemeten door multi-color antilichaam kleuring (Bourin et al., 2013). Studies in dit overzicht maakte gebruik van flow cytometrische analyse te meten oppervlak marker expressie (Müller et al., 2006; Lindroos et al., 2009; Chieregato et al., 2011; Josh et al., 2012; Trojahn Kølle et al., 2013; Bogdanova et al., 2014; Patrikoski et al., 2014).,
Trilineage Differentiatie
Differentiatie in vet, bot en kraakbeen is van oudsher gemeten met behulp van histochemical kleuringstechnieken gevisualiseerd onder microscopie; echter, de ISCT en IFATS richtlijnen aanbevolen dat kwalitatieve evaluaties moeten worden vervangen of aangevuld met kwantitatieve benaderingen zoals het meten van de lineage-specifieke mRNA expressie met behulp van reverse transcriptie kwantitatieve polymerase chain reaction (RT-qPCR) technieken (Bourin et al., 2013)., De technieken die zijn gebruikt om de differentiatiecapaciteit te meten, beschreven in de studies die in dit overzicht worden aangehaald, varieerden van histochemisch bevlekken, tot conventionele PCR en RT-qPCR. Histochemische kleuring technieken omvatten kleuring van de cellen met ofwel (1) olie rood O en Nijl rood voor adipogenese; (2) Alizarin rood s, alkalische fosfatase en von Kossa voor osteogenese; of (3) Alcian blauw en safranine voor chondrogenese (Müller et al., 2006; Kocaoemer et al., 2007; Hebert et al., 2010; Rajala et al., 2010; Koellensperger et al., 2014; Oikonomopoulos et al., 2015; Riis et al., 2016).,
Serumsuppletie
foetaal Runderserum
FBS is het traditionele serumsupplement dat wordt gebruikt voor celcultuur. FBS bevat groeifactoren (GFs) en andere elementen die essentieel zijn voor ASC gehechtheid, uitbreiding, onderhoud en proliferatie in vitro (Lennon et al., 1995, 1996; Zuk et al., 2001; van Der Valk et al., 2010). FBS is gevoelig voor batch-to-batch variatie, xenoimmunisatie, en mogelijke verontreiniging met mycoplasma, virussen, endotoxinen ,en prionen (van der Valk et al., 2004, 2010; Chieregato et al., 2011; Kyllonen et al., 2013; Jin et al., 2015)., De bron en kwaliteit van FBS kan de proliferatie en differentiatie van ASCs beïnvloeden, en routinematige screening op mycoplasma, endotoxinen en virussen is belangrijk geworden (Naaijkens et al., 2012). Deze factoren kunnen de experimentele resultaten beïnvloeden en het celproduct onveilig maken voor klinisch gebruik (Zuk et al., 2001; van Der Valk et al., 2004; Witzeneder et al., 2013).
ASC ‘ s zijn immunoprivileged, zonder de expressie van de belangrijkste histocompatibiliteitscomplex klasse II, evenals T-en B-cel costimulerende moleculen (CD80, CD86 en CD40)., De in vitro immunogeniciteit en immunosuppressieve eigenschappen van ASCs worden gewoonlijk gemeten door de ASCs samen te kweken met mononucleaire cellen in perifeer bloed in gemengde lymfocytenreacties en door de T-cel proliferatieve respons te meten (McIntosh et al., 2006; Patrikoski et al., 2014). ASC ‘ s vertonen immunomodulerende en immunosuppressieve eigenschappen, zoals blijkt uit hun vermogen om de T-celfunctie te reguleren en de cytokinesecretie in vitro en in vivo te moduleren (Leto Barone et al., 2013; Roemeling-Van Rhijn et al., 2013; Patrikoski et al., 2014)., Deze eigenschappen komen voort uit de lage immunogeniciteit van ASCs. De meerderheid van ASC en andere mesenchymale stamcel (MSc) klinische studies (Fase I, II, en III) gebruiken FBS aangevuld media, en het is gemeld dat immunogene effecten worden opgewekt door componenten van FBS in menselijke proefpersonen (Sundin et al., 2007; Riis et al., 2015). Bijvoorbeeld, een klinische studie met beenmerg-afgeleide MSCS (BM-MSCs) uitgebreid in FBS gevonden antilichamen tegen componenten van FBS (Horwitz et al., 2002)., Immuunresponsen op FBS zoals Arthus en anafylactische reacties zijn gemeld in klinische onderzoeken, waarbij patiënten werden behandeld met dendritische cellen en lymfocyten blootgesteld aan FBS (Selvaggi et al., 1997; Mackensen et al., 2000). In tegenstelling, een meta-analyse van MSC klinische studies bleek dat meer dan 75% van de experimenten gebruikt FBS in hun celuitbreidingsprotocollen en slechts één studie gecontroleerd en aangetoond bijwerkingen van FBS (Lalu et al., 2012)., In vivo onderzoeken naar de immuunrespons van muizen op ASCs toonden een behouden immunosuppressie en immunomodulatie, lage immunogeniciteit en geen reactie op FBS (Cho et al., 2009; González et al., 2009). Hoewel ASCs Uitgebreid worden getest in klinische proeven, hun definitieve gebruik als therapeutisch middel moet nog worden vastgesteld. Dit wordt nog verergerd door het gebruik van preklinische modellen die mogelijk niet biologisch relevant zijn (Monsarrat et al., 2016). Bovendien kan FBS minder immunogeen zijn bij muizen en andere diermodellen dan bij mensen., Tot slot, de immuunrespons opgewekt door FBS (Selvaggi et al., 1997; Mackensen et al., 2000; Horwitz et al., 2002) zou denkbaar de afstoting van getransplanteerde cellen in cel-gebaseerde therapie kunnen beà nvloeden.
Serumvrije alternatieven
de onbekende en ongedefinieerde samenstelling van FBS is een belangrijk nadeel. Een beter alternatief zou een chemisch gedefinieerd medium met een bekende samenstelling zijn, zoals in de handel verkrijgbare serumvrije (SF) of XF media (Usta et al., 2014)., Ten onrechte wordt aangenomen dat deze serumvrije media verstoken zijn van dierlijke producten, aangezien de termen SF en XF vaak door elkaar worden gebruikt. Echter, SF media worden meestal aangevuld met dierlijke of humane serumalbumine en GFs in ongedefinieerde hoeveelheden (Patrikoski et al., 2013). Xenovrije media daarentegen zijn chemisch gedefinieerde media die duidelijk gedefinieerde componenten in specifieke concentraties bevatten (Usta et Al., 2014).
groeifactoren
een ander alternatief voor serum is de toevoeging van GFs aan kweekmedium, hetzij afzonderlijk, hetzij als cocktail., Deze GFs kunnen synthetisch, dierlijk-afgeleid, of menselijk-afgeleid zijn. Vervanging door synthetische GFs verdient de voorkeur vanwege hun hogere kwaliteit en als gevolg van standaardisatie tussen partijen, wat mogelijk niet mogelijk is voor dierlijke of menselijke GFs. Algemeen gebruikte GFs zijn fibroblastgroeifactor, epidermale groeifactor en bloedplaatjes-afgeleide groeifactor (PDGF; Baer and Geiger, 2012; Ahearne et al., 2014). De toevoeging van GFs is in verband gebracht met een toename van de proliferatie (Hebert et al., 2010; Gharibi and Hughes, 2012)., Een verbeterde adipogene differentiatie potentieel is eerder gemeld in ASCs uitgebreid in gf aangevuld medium (Hebert et al., 2010). Nochtans, nam een andere studie een negatief effect op adipogenic en osteogenic differentiatie in op lange termijn gekweekte ASCs waar (Gharibi en Hughes, 2012).
serumalbumine
serumalbumine is een overvloedig plasma-eiwit en kan worden geïsoleerd uit mens en dier. Vaak worden SF media aangevuld met serumalbumine., Studies die humaan serumalbumine vergelijken voor ASC media suppletie hebben een verbeterde proliferatie gevonden, een kleinere spindel-achtige morfologie en een behouden differentiatie in vet, bot en kraakbeen (Rajala et al., 2010; Johal et al., 2015).
chemisch gedefinieerd XF-Medium
Xenovrij medium is aanbevolen als vervanging voor FBS en serum, aangezien het de noodzakelijke componenten voor ASC-uitbreiding bevat, geen donor-of batch-tot-batch-variatie omvat, GMP-conform is en minimale immunogeniciteit en gunstige immunosuppressie heeft (Van Der Valk et al., 2004, 2010; Usta et Al.,, 2014). Wanneer vergeleken met FBS, heeft het gebruik van XF medium voor de uitbreiding van ASCs geleid tot betere morfologische kwaliteit, verhoogde proliferatie, een vergelijkbaar immunofenotype en differentiatie in vet, bot en kraakbeen (Lindroos et al., 2009; Patrikoski et al., 2013; Oikonomopoulos et al., 2015). Het gebruik van XF media in ASC uitbreiding resulteert in ASCs verliezen hun vermogen om zich te houden aan plastic (Kyllonen et al., 2013; Patrikoski et al., 2013; Oikonomopoulos et al., 2015). Extra coatingmiddelen zijn nodig om de inherente eigenschap van kunststof-hechting geassocieerd met ASC ‘ s te behouden., In de handel verkrijgbaar XF medium is duur en het bereiden van in-house XF medium kan tijdrovend zijn en kan het risico van batch-to-batch variatie verhogen (Lund et al., 2009; Baer et al., 2010; Rajala et al., 2010; Yang et al., 2012; Kyllonen et al., 2013; Patrikoski et al., 2013; Oikonomopoulos et al., 2015).
menselijke alternatieven
menselijke alternatieven kunnen FBS en SF/XF aangevuld media vervangen en kunnen een cultuuromgeving creëren die nauwkeuriger lijkt op de menselijke omgeving (Azouna et al., 2012; Koellensperger et al., 2014)., Bovendien maakt het gebruik van autologe producten (afkomstig van hetzelfde individu) het overbodig om op infectieuze en andere ziekteverwekkers te testen.
humaan Serum
nadat volbloed in afwezigheid van een anticoagulans stolt en is gecentrifugeerd, is serum het resulterende vloeibare gedeelte dat geen bloedplaatjes, witte bloedcellen of rode bloedcellen bevat (figuur 1; Stedman, 2006). Menselijk serum (HS) kan autoloog zijn (donor en ontvanger zijn hetzelfde individu) of allogeen (afgeleid van individuen die verschillen van de ontvanger)., Zowel autologe als allogene HS zijn superieur aan FBS (Stute et al., 2004; Bieback et al., 2009, 2012; Bernardo et al., 2011; Kyllonen et al., 2013; Patrikoski et al., 2013). ASCs uitgebreid in HS hebben grotere transcriptome stabiliteit dan die uitgebreid in FBS, terwijl de genen verantwoordelijk voor verlenging van de celcyclus, differentiatie en extracellulaire matrijs en prostaglandinesynthese upregulated en overexpressed in FBS wanneer vergeleken met HS gebruikend microarray analyse (Shahdadfar et al., 2005)., ASCs uitgebreid in FBS bereikt senescentie eerder en weergegeven telomere verkorting in vergelijking met ASCs uitgebreid in HS (Shahdadfar et al., 2005). De keuze van HS schijnt weinig effect op de immunomodulatory eigenschappen van ASCs te hebben. ASCs uitgebreid in allogene HS of FBS bevattende media hadden lage immunogeniciteit en resulteerden in immunosuppressie (Patrikoski et al., 2014). ASCs uitgebreid in autologe of allogene HS vertonen Grotere proliferatie en een niet te onderscheiden immunofenotype in vergelijking met ASCs uitgebreid in FBS (Josh et al., 2012; Bogdanova et al., 2014)., ASCs uitgebreid in allogene HS zijn gedifferentieerd in vet, been en kraakbeen, hoewel de upregulation van chondrogenic en osteogenic genen werd begunstigd in vergelijking met FBS (Josh et al., 2012). ASCs uitgebreid in autologe HS zijn gedifferentieerd in vet en kraakbeen; echter, de mogelijkheid om te differentiëren in bot was minder begunstigd (Bogdanova et al., 2014). Autologe HS kan ASCs voorzien van betere proliferatie en genomische stabiliteit zoals bepaald door microarray analyse in vergelijking met allogene HS (Shahdadfar et al., 2005; Bieback et al., 2009; Bernardo et al., 2011)., ASC ‘ s uitgebreid in allogene HS ingevoerd groeistilstand en onderging celdood (Shahdadfar et al., 2005; Lindroos et al., 2009), die de potentiële voordelen van allogene HS beperkt. Hoewel autologe HS ideaal kan zijn, is de beschikbaarheid beperkt en kan er significante variatie zijn tussen patiënten in het vermogen van hun eigen serum om de groei van hun eigen cellen te ondersteunen (Lange et al., 2007). Als alternatief kunnen allogene HS worden samengevoegd, wat grotere hoeveelheden oplevert voor laboratoriumexperimenten en strenge kwaliteitscontroles door een bloedbank kan ondergaan (bijv.,, testen op de afwezigheid van infectieuze agentia en besmetting met andere bloedcellen) voorafgaand aan gebruik bij de mens (Bieback et al., 2009).
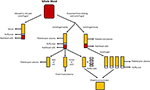
figuur 1. Productie van de verschillende menselijke alternatieven. Serum wordt geproduceerd wanneer volbloed wordt toegestaan om te stollen en gecentrifugeerd tot pellet rode en witte bloedcellen, en bloedplaatjes. Plasma wordt geproduceerd door het voorkomen van stolling gevolgd door centrifugeren., Afhankelijk van de centrifugatiesnelheid wordt ofwel bloedplaatjesarm plasma (PPP; snelle centrifugering) of bloedplaatjesrijk plasma (PRP; tragere centrifugering) geproduceerd. Als het PPP wordt bewaard bij -18°C staat het bekend als vers bevroren plasma. Bloedplaatjes concentraten kunnen worden geproduceerd, hetzij door het nemen van de bloedplaatjes slechte plasma en 4 buffy jassen en samenvoegen ze samen of centrifugeren meerdere PRP ‘ s en het samenvoegen van de bloedplaatjes pellets (gesuspendeerd in een kleine hoeveelheid plasma) samen.,
Plasma
Plasma is het niet-cellulaire vloeibare gedeelte van het bloed dat water, elektrolyten en eiwitten (stollingsfactoren, fibrinogeen en anticoagulantia) bevat. Bloedplaatjes arm plasma( PPP), vers bevroren plasma (FFP), en bloedplaatjes rijk plasma (PRP; figuur 1) kunnen worden verkregen uit volbloed door centrifugeren bij verschillende snelheden, en daaropvolgende opslag bij verschillende temperaturen. De secretie van GF kan worden versterkt door de bloedplaatjes in het volbloed te activeren met trombine voorafgaand aan centrifugatie (Doucet et al., 2005; Kocaoemer et al.,, 2007), waardoor de activiteit van de plasmaproducten wordt versterkt.
Bloedplaatjesarm Plasma
PPP is bijna vrij van bloedplaatjes en wordt geproduceerd uit volbloed door toevoeging van een anticoagulans tijdens het inzamelingsproces, waarna het plasma wordt gescheiden door middel van snelle centrifugering (figuur 1; Koellensperger et al., 2006). Hierdoor kunnen de bloedplaatjes en rode bloedcellen worden gepelleteerd. Het resulterende PPP wordt bewaard bij 4°C en wordt vers plasma genoemd., PDGF wordt uitgescheiden door de aggregerende bloedplaatjes; echter, verwaarloosbaar PDGF wordt afgegeven in PPP als gevolg van het kleine aantal resterende bloedplaatjes. GFs kan dus moeten worden toegevoegd aan PPP wanneer gebruikt in media zoals het geval is bij het gebruik van SF medium (Müller et al., 2006; Gottipamula et al., 2013). Het gebruik van PPP zonder toevoeging van GFs heeft geresulteerd in lagere proliferatiepercentages en een kleinere toename in DNA-synthese zoals gemeten met thymidine incorporatie, in vergelijking met HS en FBS (Vogel et al., 1980; Koellensperger et al., 2006)., PPP met toegevoegde GFs resulteerde in verhoogde proliferatiepercentages in vergelijking met HS (Koellensperger et al., 2006); deze verschillen zouden echter kunnen voortvloeien uit verschillende productieprotocollen van PPP en de toevoeging van verschillende niveaus van GFs aan elk van de PPP-preparaten in deze studie. Uitbreiding van ASCs in PPP resulteert in verbeterde proliferatie in vergelijking met FBS, en heeft osteogene differentiatie die vergelijkbaar is met die van ASCs uitgebreid in HS (Koellensperger et al., 2014)., Chondrogene differentiatie werd verlaagd in ASCs uitgebreid in PPP in vergelijking met ASCs uitgebreid in PRP (Koellensperger et al., 2014).
vers bevroren Plasma
FFP wordt op dezelfde wijze verkregen als PPP, maar het wordt direct na scheiding ingevroren bij -18°C (O ‘ Shaughnessy et al., 2004; Liumbruno et al., 2009). FFP is gebruikt bij de uitbreiding van BM-MSC ‘ s met positieve resultaten., Deze resultaten omvatten betere proliferatie, immunosuppressieve activiteit, en differentiatie in adipocyten en osteocyten; en een immunofenotype en morfologie die vergelijkbaar is met cellen uitgebreid in FBS (Müller et al., 2006; Mannello and Tonti, 2007). Het gebruik van FFP als serumvervanger bij ASC-uitbreiding vereist echter verder onderzoek.
Bloedplaatjesrijk Plasma
PRP is het gedeelte van het bloed dat verrijkt is met bloedplaatjes. PRP wordt geproduceerd door plasma te scheiden van rode bloedcellen bij lagere centrifugatiesnelheden, waardoor het pelleteren van de bloedplaatjes wordt voorkomen (figuur 1)., ASCs uitgebreid in PRP handhaven een klassieke immunofenotype en morfologie, en PRP verhoogt proliferatie in vergelijking met FBS (Kocaoemer et al., 2007; Chieregato et al., 2011; Atashi et al., 2015). ASC ’s uitgebreid in PRP hebben een verbeterde differentiatie-efficiëntie in de richting van adipogene en osteogene afkomst, terwijl het hebben van vergelijkbare efficiëntie voor chondrogene differentiatie, in vergelijking met ASC’ s uitgebreid in FBS (Kocaoemer et al., 2007; Chieregato et al., 2011). Bij vergelijking bleek het GS iets beter te zijn dan PRP in termen van differentiatie en proliferatie van ASC ‘ s (Kocaoemer et al.,, 2007; Chieregato et al., 2011). PRP is een slecht gedefinieerd kweekmedium supplement vanwege de hoge biologische variabiliteit en gecompliceerde extractieprocedure, waarbij het zuiveren van de bloedplaatjes factor-rijke supernatant uit plasma membranen moeilijk kan zijn. Het gebruik van PRP wordt beperkt door de grote hoeveelheden volbloed die nodig zijn om voldoende PRP voor experimenten op te leveren (Chieregato et al., 2011).,
bloedplaatjes lysaat
humaan bloedplaatjes lysaat (HPL) bevat bloedplaatjes GFs die worden verkregen door lysering van bloedplaatjes geconcentreerd in een klein volume plasma (bloedplaatjesconcentraten; figuur 1) door temperatuurschok. HPL bevat een hogere concentratie van GFs dan andere serumvervangers, waaronder humane PRP en FBS (Doucet et al., 2005; Bernardo et al., 2006, 2011; Bieback et al., 2009; Schallmoser et al., 2010)., HPL kan gemakkelijk worden verkregen en geproduceerd uit afereseproducten en buffy coats, en kan worden geresuspendeerd in PRP of een additieve oplossing (Schallmoser and Strunk, 2013; Iudicone et al ., 2014). HPL wordt geproduceerd door het invriezen van bloedplaatjes bij een temperatuur tussen -30 en -80°C gedurende 24 uur, gevolgd door een ontdooiings-en centrifugatiestap. De herhaalde bevriezen, ontdooien en centrifuge cycli zorgen voor de afgifte van GFs en de verwijdering van bloedplaatjes lichamen (Bernardo et al., 2006; Schallmoser et al., 2007)., Een ander voordeel van HPL-suppletie is dat bloedplaatjes kunnen worden gebruikt na de 4-5 dag vervaldatum van banked bloed (Bieback et al., 2009). HPL is een beter alternatief dan autologe en allogene HS, ASC ‘ s uitgebreid in HPL handhaven hun klassieke immunofenotype, differentiatie, clonogene efficiëntie, cel zuiverheid, en cel levensvatbaarheid (Trojahn Kølle et al., 2013; Riis et al., 2016). HPL ondersteunt ook uitbreiding op lange termijn zonder afbreuk te doen aan de immunomodulerende eigenschappen van ASCs, zoals gemeten door flow cytometrische analyse (Bieback et al., 2009)., Expansie in HPL resulteert in een kortere populatie verdubbelingstijd, waardoor de tijd die nodig is voor celuitbreiding wordt verminderd en de dreiging van senescentie en transformatie wordt verminderd (Doucet et al., 2005; Shahdadfar et al., 2005; Bernardo et al., 2006, 2011; Azouna et al., 2012). De bio-veiligheid van HPL is beoordeeld met behulp van array vergelijkende genomic hybridisatie en hoge gevoeligheid spectrale karyotyping, waar werd gevonden dat ASCs uitgebreid in HPL had geen chromosomale aberraties (Crespo-diaz et al., 2011; Trojahn Kølle et al., 2013)., Klassieke ASC morfologie (dun, kleiner, langwerpig, en spindel-vormige) wordt gehandhaafd in HS en HPL, terwijl ASC ‘ s uitgebreid in FBS zijn groter en minder spindel-vormige (Trojahn Kølle et al., 2013). Hoewel dit erop kan wijzen dat zowel HS als HPL selecteren voor primitieve / onrijpe ASC ‘ s (Doucet et al., 2005; Bieback et al., 2009), stelt het ook voor dat de cellen die in FBS worden gekweekt proliferatie en vooruitgang sneller naar senescentie hebben verminderd. HPL varieert tussen individuen (Bernardo et al., 2006; Crespo-diaz et al., 2011), en batch-to-batch variatie wordt verminderd wanneer HPL wordt samengevoegd (Schallmoser et al.,, 2007; Trojahn Kølle et al., 2013). Bovendien kan door het bundelen van veel donoren een grote hoeveelheid worden verkregen voor suppletie, waardoor HPL de voorkeur heeft boven PRP (Kocaoemer et al., 2007; Bieback et al., 2009; Chieregato et al., 2011).
conclusie
volgens Riis et al. van alle geregistreerde klinische proeven met uitgebreide ASCs die hun uitbreidingsvoorwaarden hebben vermeld, maakt de meerderheid gebruik van FBS, drie proeven gebruiken autologe HS, één proef gebruikt PRP, en één proef gebruikt HPL (Riis et al., 2015)., Deze statistieken zijn alarmerend, aangezien FBS het potentieel heeft om zoönotische ziekten na celtransplantatie over te dragen, en immuunreacties tegen FBS-componenten zijn gemeld (Selvaggi et al., 1997; Mackensen et al., 2000). FBS is een niet-GMP compliant product, omdat het de veiligheid en werkzaamheid van de ASC therapeutisch beïnvloedt, en dus moet worden vervangen (van der Valk et al., 2004; Kyllonen et al., 2013; Witzeneder et al., 2013). Dit is verholpen door FBS te vervangen door chemisch gedefinieerde menselijke afgeleide alternatieven., De overgang van FBS naar menselijke alternatieven of XF/SF media in de regeneratieve geneeskunde heeft het belangrijke voordeel dat de ASCs veel sneller in de laatste groeien, resulterend in een groter aantal cellen voor transplantatie in een kortere tijd. De relatieve superioriteit van verschillende cultuurmedia wordt echter nog steeds breed besproken. Studies waarbij meer dan één kweekmedium werd vergeleken, hebben wisselende resultaten opgeleverd (Lange et al., 2007; Bernardo et al., 2011; Koellensperger et al., 2014; Riis et al., 2016). Koellensperger et al., vergeleken de trilineage differentiatie van ASC ‘ s uitgebreid in FBS, PRP, PPP, en HS (Koellensperger et al., 2014). Hun resultaten toonden aan dat elk kweekmedium differentiatie in één of meer geslachten toegestaan, maar nooit in alle drie geslachten. Toen XF media, FBS en HPL aangevuld media werden vergeleken, Riis et al. gevonden dat bepaalde subpopulaties uitgedrukt specifieke oppervlakte markers afhankelijk van het cultuurmedium gebruikt (Riis et al., 2016)., Studies waarbij het immunofenotype van ASCs, uitgebreid in FBS en de andere kweekmedia, werd vergeleken, vonden weinig tot geen verschil in de expressie van de markers van het celoppervlak, ongeacht de onderzochte markers (Tabel 1). Zaaddichtheid, zuurstofspanning, samenvloeiing, dissociatie en de keuze van basale media kunnen ook experimentele resultaten beïnvloeden (Sotiropoulou et al., 2006; Freshney, 2010; Bourin et al., 2013; Inamdar and Inamdar, 2013; Feng et al., 2014; Riis et al., 2015)., De keuze van kweekmedium hangt af van de stroomafwaartse toepassing van deze cellen (toediening van gedifferentieerde of niet-gedifferentieerde ASCs) en de aandoening die wordt behandeld. Bovendien moet de immunogeniciteit van het kweekmedium dat wordt gebruikt om de cellen vóór klinische toepassing uit te breiden, worden beschouwd als een parameter die de klinische uitkomst kan beïnvloeden. In de meeste studies waarbij verschillende kweekmedia werden vergeleken, werden de criteria van het ISCT en het IFATS gebruikt om het gebruik van een alternatief voor FBS te valideren., De meeste van deze studies onderzoeken ASC morfologie, proliferatie, immunophenotype, en de capaciteit van deze cellen om langs osteogenic, chondrogenic, en adipogenic lijnen in verschillende cultuurmedia te onderscheiden. Weinig studies hebben andere aspecten van ASCs, zoals senescentie, genetische stabiliteit, transcriptoom, proteoom, immunogeniciteit, cytokine secretie, en celcyclus onderzocht (Shahdadfar et al., 2005; Bieback et al., 2012). Terwijl de criteria van ISCT en IFATS een poging waren om het gebied te verenigen in termen van standaard operationele procedures (Dominici et al., 2006; Bourin et al.,, 2013), bestaat er geen consensus rond welke eigenschappen van ASCs relevant zijn voor klinische proeven, waardoor de vergelijking van verschillende kweekmedia vrijwel onmogelijk is. Hoewel deze criteria meetbare resultaten bieden voor eenvoudige vergelijking, kunnen veranderende componenten die worden gebruikt voor de uitbreiding van ASC ‘ s verschillende effecten hebben op de veiligheid, werkzaamheid en reproduceerbaarheid van ASC-eindproducten. Het onderzoeken van veranderingen in transcriptome, proteome, en secretome van ASCs uitgebreid in diverse cultuurmedia is belangrijk, zoals het gebruik van cellen uitgebreid onder variërende voorwaarden in aangewezen preclinical modellen is.,

Tabel 1. De effecten van de verschillende media supplementen op ASCs in vitro.
Auteursbijdragen
CD conceptualiseerde en stelde de recensie op, en keurde het definitieve manuscript goed. MP assisteerde bij de conceptualisering van de review, reviseerde en keurde het definitieve manuscript goed. MRO assisteerde bij de conceptualisering van het overzicht, redigeerde en keurde het definitieve manuscript goed, en verhoogde de financiering voor de betrokken projecten. Alle auteurs hebben het definitieve manuscript gelezen en goedgekeurd.,
financiering
Dit onderzoek en de publicatie daarvan zijn het resultaat van financiering door de Medical Research Council of South Africa in termen van (a) The MRC ‘ s Flagships Awards Project SAMRC-RFA-UFSP-01-2013/stamcellen en (b) de extramurale eenheid voor stamcelonderzoek en-therapie. De National Research Foundation of South Africa heeft ook financiering verstrekt.
belangenconflict verklaring
De auteurs verklaren dat het onderzoek werd uitgevoerd zonder enige commerciële of financiële relatie die als een potentieel belangenconflict kon worden opgevat.,
Dankbetuigingen
De auteurs willen Dr. Cheryl Tosh bedanken voor haar redactionele hulp.
Chieregato, K., Castegnaro, S., Madeo, D., Astori, G., Pegoraro, M., and Rodeghiero, F. (2011). Epidermale groeifactor, basisfibroblastgroeifactor en bloedplaatjes-afgeleide groeifactor-bb kunnen foetaal runderserum vervangen en concurreren met humaan bloedplaatjesrijk plasma in de ex vivo expansie van mesenchymale stromale cellen afgeleid van vetweefsel. Cytotherapie 13, 933-943. doi: 10.3109 / 14653249.2011.,583232
PubMed Abstract / CrossRef Full Text/Google Scholar
Mannello, F., and Tonti, G. (2007). Beknopte beoordeling: Geen doorbraken voor menselijke mesenchymale en embryonale stamcelcultuur: geconditioneerde medium, feeder laag, of feeder-vrij; medium met foetale kalf serum, menselijk serum, of verrijkt plasma; serum-vrij, serum vervanging niet geconditioneerde medium, of ad hoc formule? alles wat schittert is geen goud! Stamcellen 25, 1603-1609. doi: 10.1634 / stemcells.2007-0127
PubMed Abstract / CrossRef Full Text / Google Scholar
Selvaggi, T. A., Walker, R. E.,, and Fleisher, T. A. (1997). Ontwikkeling van antilichamen tegen foetaal kalfsserum met arthusachtige reacties bij met humaan immunodeficiëntievirus geïnfecteerde patiënten die syngene lymfocyteninfusies krijgen. Bloed 89, 776-779.
PubMed Abstract/Google Scholar
Stedman, T. L. (2006). Stedman ‘ s Medisch Woordenboek. Philadelphia, PA: Lippincott Williams & Wilkins.
Google Scholar