Rutherford i Manchester, 1907-1919
Ernest Rutherford upptäckte atomens kärna 1911. Vi läser detta i läroböcker och i populära skrifter. Men vad betyder det uttalandet? Geografisk upptäckt innebär vanligtvis att man ser en plats för första gången. Men kan upptäckten vara densamma för ett rike dolt ur sikte? Man kan inte se en atom i den meningen., Så det här antyder att kanske historien om upptäckten av kärnan var mer komplicerad. Historien som den utvecklades i Rutherfords labb vid universitetet i Manchester kretsade kring riktiga människor. Det innebar frustrationer och triumfer. Det involverade hårt arbete och förvirring och inspiration.
 när Rutherford blev professor i Manchester 1907 hittade han moderna laboratorier för både undervisning och forskning. På uppmaning av sin föregångare, Arthur Schuster, höjdes över £40,000 för att ge fysikprogrammet. Som jämförelse var Rutherfords generösa lön £1,600 / år., Kredit: från boken: The physical laboratories of the University of Manchester: ett rekord på 25 års arbete av University of Manchester, Manchester: vid University Press, 1906. AIP Emilio Segrè visuella Arkiv, spröda böcker samling.
när Rutherford blev professor i Manchester 1907 hittade han moderna laboratorier för både undervisning och forskning. På uppmaning av sin föregångare, Arthur Schuster, höjdes över £40,000 för att ge fysikprogrammet. Som jämförelse var Rutherfords generösa lön £1,600 / år., Kredit: från boken: The physical laboratories of the University of Manchester: ett rekord på 25 års arbete av University of Manchester, Manchester: vid University Press, 1906. AIP Emilio Segrè visuella Arkiv, spröda böcker samling.
Rutherford anlände till Manchester sommaren 1907, månader innan universitetets mandatperiod började. Han hade fått namnet Langworthy Professor i Fysik, efterföljaren till Arthur Schuster (1851-1934), som gick i pension vid en ålder av 56 för att rekrytera Rutherford. Schuster hade byggt en modern fysik byggnad, anlitade Hans Geiger, Ph D., (1882-1945) på grund av hans experimentella skicklighet, och gav en ny position i matematisk fysik för att runda ut ett fullständigt fysikprogram. Rutherford kom in i mitten av fysikvärlden. Forskare kom till honom av dussinet.
Rutherford kom med många forskningsfrågor i åtanke. Han var inte klar med pusselarna i toriums, radiums sönderfallsfamiljer etc., men han gick mycket av detta arbete till Boltwood, Hahn och Soddy. Boltwood och Hahn arbetade båda med Rutherford i Manchester, Boltwood 1909-1910 och Hahn 1907-1908., Rutherford vände gradvis sin uppmärksamhet mycket mer till A (alfa), β (beta) och γ (gamma) strålar själva och vad de kan avslöja om atomen. Det vill säga, han lämnade radiokemi till andra och vände sig till fysiken.
 Rutherford samlade alltid en grupp ljusa unga forskare runt honom. I denna gruppfoto av 1910 är Ernest Marsden och Hans Geiger. Front and center är professorer Schuster och Rutherford, och centrerad på baksidan är William Kay, den begåvade och hjälpsamma laboratoriet steward. Kredit: J. B. Birks, ed., Davidson Manchester (London: Heywood & Co., 1962), motsatt s.38.
Rutherford samlade alltid en grupp ljusa unga forskare runt honom. I denna gruppfoto av 1910 är Ernest Marsden och Hans Geiger. Front and center är professorer Schuster och Rutherford, och centrerad på baksidan är William Kay, den begåvade och hjälpsamma laboratoriet steward. Kredit: J. B. Birks, ed., Davidson Manchester (London: Heywood & Co., 1962), motsatt s.38.
Rutherfords tidiga lag i Manchester inkluderade Geiger och William Kay (1879-1961), junior laboratorieassistent sedan 1894. Rutherford befordrade Kay till laboratory steward i 1908, att hantera labbutrustning och att hjälpa honom i sin forskning. År 1957 tänkte Kay tillbaka till sin ungdom med Rutherford i en intervju. Språket är pittoreskt, men beskrivningen är så nära Rutherfords tillvägagångssätt som vi får., Frågeställaren var Samuel Devons (1914-2006), som var en av Rutherford förra studenter på 1930-talet.
 Hans Geiger var Rutherford viktigaste partner i alfa-ray forskning från 1907 till 1913. Tillsammans utvecklade de flera sätt att upptäcka alfastrålar. De visade alfastrålar är dubbelt joniserade heliumkärnor. Ca. 1908. Kredit: AIP Emilio Segre visuella Arkiv, fysik idag samling.
Hans Geiger var Rutherford viktigaste partner i alfa-ray forskning från 1907 till 1913. Tillsammans utvecklade de flera sätt att upptäcka alfastrålar. De visade alfastrålar är dubbelt joniserade heliumkärnor. Ca. 1908. Kredit: AIP Emilio Segre visuella Arkiv, fysik idag samling.
Rutherford och Hans Geiger arbetade nära 1907 och 1908 på detektion och mätning av α-partiklar., Om de skulle använda α-partiklar för att sondera atomen, hade de först veta mer om dessa partiklar och deras beteende. Rutherford hade försökt och misslyckats tillbaka på McGill att räkna α partiklar.
ett år senare i Manchester lyckades han och Geiger med två metoder för att observera α-partiklar. Den första metoden involverade scintillationer upphetsade av A-partiklar på ett tunt lager av zinksulfid. De observerade dessa genom ett mikroskop och räknade scintillationerna i olika spridningsvinklar., De utvecklade också en ”elektrometer” som kunde visa passagen av en enskild α-partikel till en stor publik. Instrumentet, som utvecklades till” Geiger-räknaren”, hade en delvis evakuerad metallcylinder med en tråd ner i mitten. De applicerade en spänning mellan cylindern och tråden tillräckligt hög nästan för att gnista. De medgav α-partiklar genom ett tunt glimmerfönster, där dessa partiklar kolliderade med gaser och producerade gasjoner. Dessa kolliderade sedan med andra molekyler och producerade fler joner, och så vidare., Varje α-partikel producerade en kaskad av joner, som delvis tömde cylindern och indikerade passage av en a-partikel. Geiger och Rutherford publicerade flera artiklar 1908 och 1909 om dessa metoder och deras användning.
Rutherford skrev till Henry Bumstead (1870-1920), en amerikansk fysiker, den 11 juli 1908:
Geiger är en bra man och arbetade som en slav. Jag kunde aldrig ha hittat tid för trusket innan vi fick saker att gå i bra stil. Slutligen gick allt bra, men spridningen är djävulen. Vårt rör fungerade som en charm och vi kunde lätt få ett kast på 50 mm., för varje partikel. … Geiger är en demon i arbetet med att räkna scintillationer och kunde räkna med intervaller för en hel natt utan att störa hans jämlikhet. Jag fördömde kraftigt och gick i pension efter två minuter. (Citerad i Eve, s. 180.)
Även om Rutherford misstänkte så tidigt som 1906 att α-partiklar var heliumatomer avskalade från sina elektroner, krävde han en hög standard på bevis. Ett slags experiment var inte tillräckligt. En slags detektor räckte inte. Han ville ha fler bevis., För detta önskade Rutherford ”stora spänningar” och stora elektromagneter för att avleda α-partiklar, men den här metoden var ännu inte mogen. Lab steward William Kay återkallade i den citerade muntliga historieintervjun att Rutherford 1908 insisterade på att starka elektriska och magnetiska fält behövdes för att mäta mer direkt laddningen och massan av α Och β-partiklarna:
Kay sa att Rutherford ville ha en stor, vattenkyld magnet, men att han ”tappade den som en varm kaka” när han lärde sig kostnaden. Så han behövde en ny attack. Den nya linjen var väldigt enkel, en kemisk procedur blandad med fysik., För detta arbete rekryterade Rutherford Thomas Royds (1884-1955), som hade fått sin fysik hedersexamen 1906. De samlade α-partiklar i ett förseglat glasrör, komprimerade dem och passerade en elektrisk gnista genom. De studerade det emitterade ljuset i ett spektroskop och fann att det var identiskt med heliumspektrumet. Inom några månader tilldelades Rutherford Nobelpriset för kemi, ” för hans undersökningar av upplösningen av elementen och kemin av radioaktiva ämnen.,”(Nobel citation) Rutherford och Royds hade fastställt identiteten och de primära egenskaperna hos α-partiklar. Rutherford vände sin uppmärksamhet på att använda dem för att sondera atomen.
hösten 1908 började en viktig serie undersökningar. Geiger hade passerat balkar av α-partiklar genom guld och andra metalliska folier, med hjälp av de nya detektionsteknikerna för att mäta hur mycket dessa balkar dispergerades av atomerna i folierna. Geiger trodde Ernest Marsden (1889-1970), en 19-årig student i Hedersfysik, var redo att hjälpa till med dessa experiment och föreslog det till Rutherford., Eftersom Rutherford ofta drev tredjeårsstudenter till forskning och sa att detta var det bästa sättet att lära sig om fysik, kom han lätt överens.
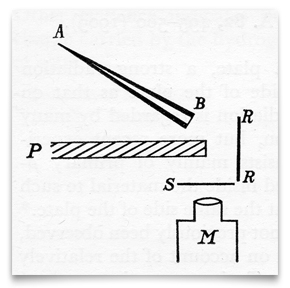 den här skissen, från Geiger och Marsdens 1909-artikel, visar ett koniskt glasrör fullt av ”radium emanation” (radon), stängt vid B med en tunn ruta av glimmer. Detta var deras källa till Alfa (α) partiklar. S var en zinksulfidskärm, som scintillerade när den slogs av en a-partikel. P var en blyskärm, som blockerade Alla α-partiklar från att resa direkt till zinksulfidskärmen., RR var en folie (eller folier) av olika metaller (inklusive guld) som ”diffust reflekterade” infallande α partiklar. Geiger och Marsden observerade de resulterande scintillationerna genom ett observationsmikroskop, M. Credit: H. Geiger och E. Marsden, ”på en diffus reflektion av α-partiklarna”, Proceedings of the Royal Society, 1909, 82: 495-500.
den här skissen, från Geiger och Marsdens 1909-artikel, visar ett koniskt glasrör fullt av ”radium emanation” (radon), stängt vid B med en tunn ruta av glimmer. Detta var deras källa till Alfa (α) partiklar. S var en zinksulfidskärm, som scintillerade när den slogs av en a-partikel. P var en blyskärm, som blockerade Alla α-partiklar från att resa direkt till zinksulfidskärmen., RR var en folie (eller folier) av olika metaller (inklusive guld) som ”diffust reflekterade” infallande α partiklar. Geiger och Marsden observerade de resulterande scintillationerna genom ett observationsmikroskop, M. Credit: H. Geiger och E. Marsden, ”på en diffus reflektion av α-partiklarna”, Proceedings of the Royal Society, 1909, 82: 495-500.
Geiger och Marsden började med liten vinkeldispersion och försökte olika tjocklekar av folier, söker matematiska relationer mellan spridning och tjocklek av folie eller antal atomer korsade., Marsden senare påminde om att Rutherford sade till honom mitt i dessa experiment: ”se om du kan få någon effekt av alfa-partiklar direkt reflekteras från en metallyta.”(Rapporteras av Marsden i Birks, 1962, s. 8). Marsden tvivlade på att Rutherford förväntade sig tillbaka spridning av α-partiklar, men som Marsden skrev
…det var en av de ”hunches” som kanske någon effekt kan observeras, och att i vilket fall som helst att grannområde av denna Tom tiddlers mark kan utforskas av rekognosering., Rutherford var någonsin redo att möta det oväntade och utnyttja det, där gynnsamt, men han visste också när man skulle sluta på sådana utflykter. (Birks, 1962, s. 8)
detta var Rutherfords lekfulla tillvägagångssätt i handling. Hans elever och andra försökte ut sina idéer, varav många var återvändsgränder. Denna idé att leta efter backscattering av α partiklar, dock lönat sig., Rutherford skrev:
Experiment, regisserad av den disciplinerade fantasin, antingen av en individ eller, ännu bättre, av en grupp individer med varierande mentala utsikter, kan uppnå resultat som långt överskrider fantasin ensam av den största filosofen. (Citerad i Eve, 1939, Frontmatter)
någon gång senare i 1908 eller 1909 sa Marsden att han rapporterade sina resultat till Rutherford. Rutherford påminde om detta lite annorlunda:
Jag minns …senare kommer Geiger till mig i stor spänning och säger: ”vi har kunnat få några av A-partiklarna att komma bakåt…,”Det var den mest otroliga händelse som någonsin hänt mig i mitt liv. Det var nästan otroligt som om du sköt ett 15-tums skal på en bit mjukpapper och det kom tillbaka och slog dig. (Rutherford, 1938, s. 68)
mänskligt minne är fallibelt. Oavsett om Marsden eller Geiger berättade för Rutherford, var effekten densamma. Rutherford sa att de skulle förbereda en publikation från denna forskning, som de lämnade in i maj 1909. Dessutom började detta Rutherford tänka mot vad i slutändan, nästan två år senare, publicerade han som en teori om atomen.,
vad gjorde Rutherford för resten av 1909 och hela 1910? För en sak var hans nära vän Boltwood i Manchester för läsåret som arbetade med Rutherford på radioaktiva sönderfallsprodukter av radium. Han granskade och talade också om tidigare idéer om atomstruktur. Viktigast, han tog fenomenet spridning av A-partiklar systematiskt och testade varje bit. Rutherford hade inte sin djärva idé — kärnatomen-omedelbart, men han kom till det gradvis genom att överväga problemet från många håll.,
hösten 1910 tog han Marsden tillbaka till Manchester för att slutföra rigorös experimentell testning av sina idéer med Geiger. De återupprättade utsläppshastigheterna och α-partiklarnas intervall från radioaktiva källor och undersökte sina statistiska analyser på nytt. Rutherford försökte förena spridningsresultat med olika atommodeller, särskilt J. J. Thomsons, där den positiva elen betraktades som dispergerad jämnt över hela atomens sfär.
 en sida av Rutherfords tidiga, odaterade (1910 eller 1911), grova anteckningar., De första raderna läser: ”teori om atomens struktur. Antag att atom består av + laddning ne vid Centrum & av – laddning som elektron fördelad över hela radien r. ” han utarbetade sedan idéer om beräkningen av avböjningskraften på en laddad partikel som passerar nära detta laddade centrum. Kredit: J. B. Birks, ed. Davidson Manchester (London: Heywood & Co., 1962), s.70.
en sida av Rutherfords tidiga, odaterade (1910 eller 1911), grova anteckningar., De första raderna läser: ”teori om atomens struktur. Antag att atom består av + laddning ne vid Centrum & av – laddning som elektron fördelad över hela radien r. ” han utarbetade sedan idéer om beräkningen av avböjningskraften på en laddad partikel som passerar nära detta laddade centrum. Kredit: J. B. Birks, ed. Davidson Manchester (London: Heywood & Co., 1962), s.70.
vid någon tidpunkt på vintern 1910-1911 utarbetade Rutherford den grundläggande idén om en atom med ett ”laddat centrum”.,”Som Geiger och Marsden påpekade i sin 1909-artikel:
Om α-partikelns höga hastighet och massa beaktas, verkar det förvånande att några av α-partiklarna, som experimentet visar, kan vändas inom ett lager av 6 x 10-5 cm. av guld genom en vinkel på 90°, och ännu mer. För att producera en liknande effekt av ett magnetfält skulle det enorma fältet 109 absoluta enheter krävas. (Birks, s. , 179)
Rutherford avslutade i sitt maj 1911-papper att en sådan anmärkningsvärd avvikelse i vägen för en massiv laddad partikel endast kunde uppnås om det mesta av massan av, säg, en atom av guld och det mesta av dess laddning koncentrerades i en mycket liten central kropp. Obs! vid denna tidpunkt 1911 kallade Rutherford inte detta en ” kärna.”
Du behöver Flash Player installerad för att lyssna på detta ljudklipp.,
Rutherfords första offentliga tillkännagivande av kärnteorin gjordes vid ett möte i Manchester Literary and Philosophical Society, och han uppmanade oss unga pojkar att gå till mötet. Han sa att han hade några intressanta saker att säga och han trodde att vi skulle vilja höra dem. Vi visste inte vad det handlade om då. De äldre i laboratoriet visste naturligtvis Geiger och Marsden eftersom de redan gjorde experimenten. I själva verket, om de inte hade gjort några som var tillräckliga för att vara avgörande, Rutherford nämnde aldrig det offentligt., Och självklart visste Darwin om det mycket tidigare. Men det måste ha varit tidigt 1911, och vi gick till mötet och han berättade för oss. Och han nämnde då att det fanns några experimentella bevis som hade erhållits av Geiger och Marsden. Han sa inte, såvitt jag minns, mer om resultaten än att de var ganska avgörande. Och, som jag sa tidigare, han skulle aldrig ha gjort ett offentligt tillkännagivande av detta slag om han inte hade haft goda bevis., Och det är en av de egenskaper som går igenom alla Rutherfords arbete, särskilt allt hans arbete fram till slutet av Manchester-perioden. Om man tittar på några av hans papper i början — jag kallar McGill de tidiga dagarna — var han ganska övertygad om att alfapartiklarna var atomer av helium, men han sa aldrig det med dessa ord. Han sa alltid att de var antingen atomer av helium eller molekyler av väte eller kanske han kan ha sagt något annat av den vikten., Det var ganska karakteristiskt för honom att han aldrig skulle säga något var så om han inte hade experimentella bevis för det som verkligen tillfredsställde honom.
i själva verket var Rutherford ytterst försiktig med att dra slutsatser om denna centrala laddning: ”en enkel beräkning visar att atomen måste vara en plats för ett intensivt elektriskt fält för att producera en så stor deflexion vid ett enda möte.”(Birks, s. 183). Han arbetade snabbt och grovt att flera kvantitativa relationer skulle vara sanna om denna grundläggande teori var korrekt., För det första bör antalet α-partiklar som sprids genom en given vinkel vara proportionell mot foliens tjocklek. För det andra bör detta nummer stå i proportion till kvadraten på kärnladdningen. Slutligen bör det vara omvänt proportionellt mot den fjärde kraften i α-partikelns hastighet. Dessa tre idéer lade fram det experimentella programmet Geiger och Marsden för nästa år.
Du behöver Flash Player installerad för att lyssna på detta ljudklipp.,
Rutherfords intresse var då nästan helt i forskningen. Han hade undervisat väldigt lite i McGill. Han var forskningsprofessor. Jag antar att han gav några föreläsningar men det skulle ha varit väldigt få. Och hans intresse var helt naturligt på forskningssidan. Han gav några föreläsningar, men elementära föreläsningar, den typ av sak du förväntar dig att en man ska veta innan han kom till universitetet. De var föreläsningarna till ingenjörerna. Rutherford kunde hålla dem under kontroll., Det fanns kanske bara en annan man på avdelningen som kunde ha gjort det, och han (Rutherford?) njöt av dem eftersom han kunde visa dem de mycket intressanta experimenten man kan utföra i grundkurser.
det har ofta sagts till mig att Rutherford var en dålig föreläsare. Jag har aldrig hört sånt nonsens. Det är helt sant att han ibland skulle vara lite tråkig, lite blandad, men det var bara vid mycket sällsynta tillfällen. Det fanns andra tillfällen då han verkligen var mest stimulerande. Det var en enorm entusiasm om honom.,
Rutherford underhöll möjligheten att det laddade centret är negativt. Det låter konstigt idag, så vad gjorde det rimligt? För det första var det inte så annorlunda än Thomsons modell. För det andra, eftersom Rutherford visste att α-partiklar bär en dubbel + laddning, trodde han att detta skulle kunna fungera på samma sätt som solen gör på en komet som sveper nära den. Det skulle slingshot a partikeln runt och tillbaka mot dess källa. Han ansåg också en nästan bortglömd modell som föreslagits av den japanska fysikern Hantaro Nagaoka (1865-1950) — den Saturniska modellen., Nagaoka och Rutherford var i kontakt 1910 och 1911 och Rutherford nämnde Nagaokas modell av ”en central lockande massa surround av ringar av roterande elektroner” (Birks, s. 203). Slutresultatet i detta kritiska Rutherford-papper var dock Rutherfords tillkännagivande att huruvida atomen var en disk eller en sfär, och faktiskt om den centrala laddningen var positiv eller negativ, inte skulle påverka beräkningarna. Rutherford var alltid noga med att inte hävda mer än hans resultat kunde stödja.,
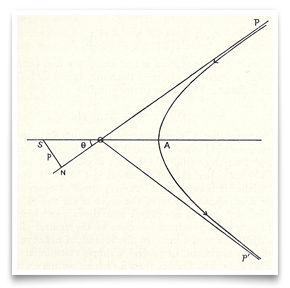 I Rutherfords nu berömda papper från maj 1911 om spridning av alfa partiklar av guldfolie, han inkluderade denna skiss av hyperbolisk väg av en partikel. Kredit: E. Rutherford, ”spridningen av α Och β-partiklar efter Materia och materiens struktur”, Philosophical Magazine, 1911, 21: 669-688.
I Rutherfords nu berömda papper från maj 1911 om spridning av alfa partiklar av guldfolie, han inkluderade denna skiss av hyperbolisk väg av en partikel. Kredit: E. Rutherford, ”spridningen av α Och β-partiklar efter Materia och materiens struktur”, Philosophical Magazine, 1911, 21: 669-688.
Rutherford såg möjliga tester av den centrala laddningens Art. Absorptionen av p-partiklar, sade han, bör vara annorlunda med ett negativt centrum jämfört med en positiv., Ett positivt centrum skulle förklara den stora hastighet som α-partiklar uppnår under utsläpp från radioaktiva element. Men det var bara tips.
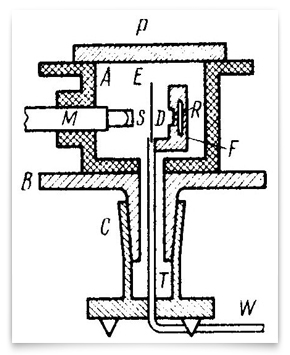 detta schema representerar de raffinerade experiment av 1912-13 genomförs av Geiger och Marsden. R var källan till alfapartiklar, e var guldfolien, och M var mikroskopet roterbart runt en vertikal axel centrerad på guldfolien. Alfa partiklar från källan passerade genom membranet D, utspridda av folien, och observerades som scintillations på skärmen S., Geiger och Marsden observerade vinklarna för spridda partiklar genom att rotera mikroskopskärmsmonteringen. Kredit: H. Geiger och E. Marsden, ”Lagar Deflexion av α-Partiklar med Stora Vinklar,” Filosofisk Tidskrift 1913, 25:604-623.
detta schema representerar de raffinerade experiment av 1912-13 genomförs av Geiger och Marsden. R var källan till alfapartiklar, e var guldfolien, och M var mikroskopet roterbart runt en vertikal axel centrerad på guldfolien. Alfa partiklar från källan passerade genom membranet D, utspridda av folien, och observerades som scintillations på skärmen S., Geiger och Marsden observerade vinklarna för spridda partiklar genom att rotera mikroskopskärmsmonteringen. Kredit: H. Geiger och E. Marsden, ”Lagar Deflexion av α-Partiklar med Stora Vinklar,” Filosofisk Tidskrift 1913, 25:604-623.
Geiger och Marsden arbetade faktiskt systematiskt genom de testbara konsekvenserna av Rutherfords centrala laddningshypotes. Den första stora publikationen av deras resultat var på tyska i arbetet i Wien Academy of Sciences (Sitzungberichte der Wiener Akademie der Wissenschaften) 1912., Denna 30-sidiga version följdes av en på engelska 1913 i den filosofiska tidningen: ”lagarna för deflexion av α-partiklar genom stora vinklar” den engelska versionen är den mer kända. Små skillnader mellan de två ledde en historiker att föreslå att Rutherford bestämde sig för ett positivt laddat center i augusti 1912 (Trenn, 1974). Rutherford andra gruppmedlemmar, speciellt Charles Galton Darwin (1887-1962), H. G. J. Moseley (1887-1915), och Niels Bohr (1885-1962) var en framträdande fråga i det slutliga upprättandet av Rutherford kärnkraft atom.,
 Den unge Henry G. J. Moseley, i människans historia-Trinity Laboratorium, Oxford, ca. 1910. Senare samma år började Moseley forskning i Rutherfords Manchester lab. Hans lysande karriär avbröts i strid under andra Världskriget. Kredit: Oxford University, Museum of the History of Science, artighet AIP Emilio Segrè Visual Arkiv, Fysik Idag Samling.
Den unge Henry G. J. Moseley, i människans historia-Trinity Laboratorium, Oxford, ca. 1910. Senare samma år började Moseley forskning i Rutherfords Manchester lab. Hans lysande karriär avbröts i strid under andra Världskriget. Kredit: Oxford University, Museum of the History of Science, artighet AIP Emilio Segrè Visual Arkiv, Fysik Idag Samling.
det ”stora kriget” störde helt arbetet i Rutherfords Manchester-avdelning. Bohr återvände till Danmark. Marsden accepterade en professur i Nya Zeeland. Moseley dog i slaget vid Gallipoli., James Chadwick (1891-1974), som arbetade med Geiger vid Tekniska Universitetet i Berlin när kriget bröt ut, tillbringade flera år praktiserat i Ruhleben läger för krigsfångar. Andra studenter gick ut i krig också, och Rutherford ägnade stor energi till att mobilisera vetenskap för krigsinsatsen och specifikt till anti-ubåtstekniker.
 Niels Bohr arbetade först med Rutherford på
Niels Bohr arbetade först med Rutherford på
Manchester 1912. Detta foto visar de unga Niels och Margrethe Bohr, ca., 1914, när Bohr lyckats Charles Galton Darwin som Schuster Läsare i Matematisk Fysik vid Manchester. Kredit: AIP Emilio Segre Visual Arkiv, Margrethe Bohr Samling.
mot denna distraherade bakgrund började Rutherford och hans lab steward, William Kay, 1917 att utforska passage av α-partiklar genom väte, kväve och andra gaser. När det stora kriget slutade hjälpte Ernest Marsden kort med de tråkiga scintillationsobservationerna som gav ledtrådar till kärnans natur. Rutherford rapporterade de preliminära resultaten av dessa omfattande experiment 1919., Rutherford placerade en källa till radium C (vismut-214) i en förseglingsbar mässingsbehållare, monterad så att källans position kan ändras och så att olika gaser kan införas eller ett vakuum produceras, efter önskemål. A-partiklarna korsade behållarens inre och passerade genom en slits, täckt av en silverplatta eller annat material och slog en zinksulfidskärm, där en scintillation observerades i ett mörkt rum. När vätgas infördes i behållaren och försiktighet togs för att absorbera α-partiklarna innan de slog på skärmen, observerades scintillationer fortfarande., Rutherford ansåg att när α-partiklarna passerade vätegasen kolliderade de ibland med vätekärnor. Som Rutherford skrev, producerade detta ”snabba väteatomer” som mestadels projicerades framåt i riktning mot α-partiklarnas ursprungliga rörelse.
Rutherford hade flera subtila frågor i åtanke under dessa experiment, främst berörda av kärnans natur., Han bad sin kollega Darwin att analysera dessa kollisioner baserat på en ”enkel teori” av elastiska kollisioner mellan punktkärnor som avstöts enligt en omvänd kvadratisk lag, α-partiklarna som bär en laddning av 2 gånger en elektron (och motsatt tecken) och vätekärnorna 1 gånger. Darwin fann att ALLA α-partiklar närmar sig inom 2, 4×10-13 cm skulle producera en ” snabb väteatom.”Denna enkla teori förutspådde dock betydligt färre accelererade väteatomer än vad som observerades i experimenten.,
Rutherford avvisade förklaringar av denna varians baserat på olika avgifter på partiklarna eller andra lagar än inversa fyrkantiga lagar. Snarare drog han slutsatsen att för avstånd i storleksordningen av elektronens diameter kan ” heliumkärnans struktur inte längre betraktas som en punkt…”. Han ansåg att heliumkärnan (α-partikeln) har en komplex struktur av fyra vätekärnor plus två negativt laddade elektroner. (Vi skulle säga att den består av två protoner.,) Rutherford drog slutsatsen att deformation av komplexa kärnor under kollisioner var en mer sannolik förklaring, variationen av krafterna mellan kärnorna varierar på ett komplext sätt på nära håll.
med hänsyn till de intensiva krafterna som tas upp i sådana kollisioner skulle det inte vara förvånande om heliumkärnan skulle bryta upp. Inga tecken på en sådan upplösning…har observerats, vilket tyder på att heliumkärnan måste vara en mycket stabil struktur.,
Vi måste komma ihåg att Rutherford inte direkt kunde observera kärnans struktur, så hans slutsatser var preliminära. Ändå övervägde han öppet möjligheterna till en komplex kärna, som kunde deformeras och till och med av eventuell sönderdelning. Dessa tankar formade denna intensiva period av experimentella undersökningar.