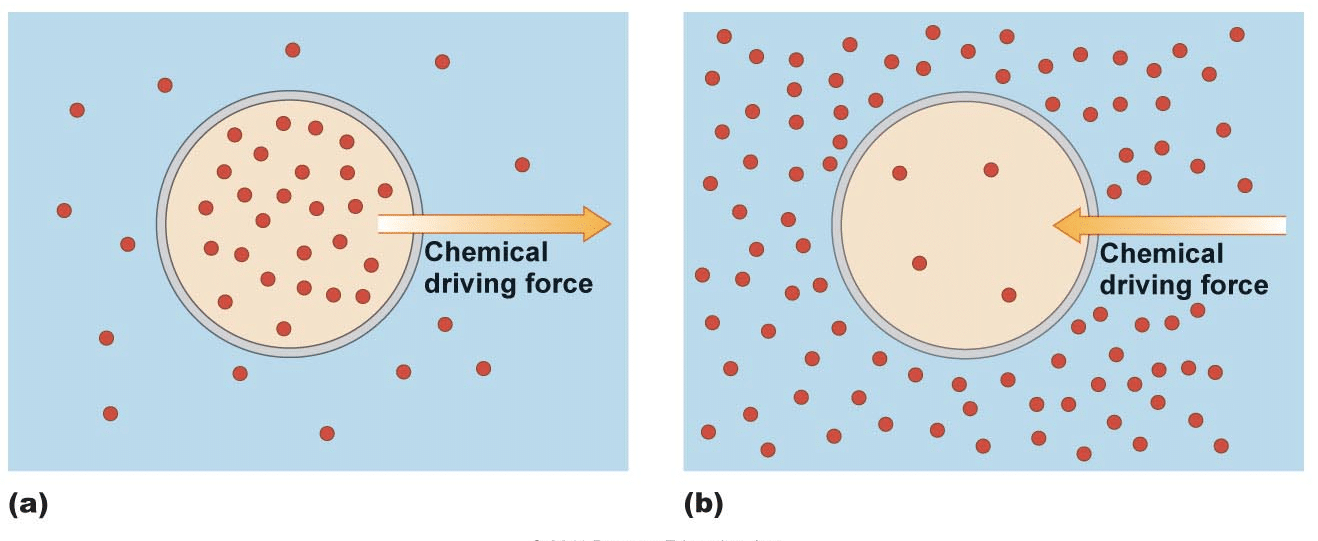
la definición formal de un gradiente de concentración es el proceso de partículas, que a veces se llaman solutos, que se mueven a través de una solución o gas desde un área con un mayor número de partículas a un área con un menor número de partículas. Las áreas están típicamente separadas por una membrana. Esta membrana puede ser permeable, semipermeable o no permeable., Permeable se define como una membrana que puede ser atravesada por partículas, iones o agua. Semipermeable significa que algunas partículas, iones o agua pueden atravesar la membrana. Finalmente, una membrana no permeable significa que ninguna partícula, iones o agua puede atravesar la membrana.
un ejemplo que podría ayudarlo a comprender los diferentes tipos de membranas sería diferentes tipos de cercas. Una valla de madera permitiría que muchas cosas pasaran – esto sería un ejemplo de una membrana permeable., Una cerca de eslabones de cadena permitiría que algunos artículos pequeños pasaran a través de ella, esto sería como una membrana semipermeable. Una valla de plástico sólido no permitiría que los elementos pasen a través de ella en absoluto-esto representaría una membrana no permeable.

La función de los Gradientes de Concentración
gradientes de Concentración son una consecuencia natural de las leyes de la física., Sin embargo, los seres vivos han encontrado muchas maneras de utilizar sus propiedades para lograr importantes funciones de la vida. Los organismos que necesitan mover una sustancia dentro o fuera de sus células, por ejemplo, pueden utilizar el movimiento de una sustancia por su gradiente de concentración para transportar otra sustancia en tándem.
los organismos también pueden usar gradientes de concentración para lograr cambios o movimientos repentinos al liberar altas concentraciones de soluto para moverse a áreas de baja concentración. Las neuronas son un ejemplo de células que utilizan altas concentraciones de solutos para lograr cambios rápidos.,
ejemplos cotidianos de gradiente de concentración
la concentración de moléculas de olor es más alta en áreas de la piel que han tenido perfume o aftershave aplicado directamente. Otros pueden oler el olor porque algunas de esas moléculas siempre se alejan de la persona perfumada, la fuente, hacia el aire, moviéndose por el gradiente de concentración, de una concentración alta a una concentración más baja. Con el tiempo, las moléculas aromáticas están tan dispersas que ya no se pueden detectar.,
piense en el olor desagradable del hedor skunk, cuando un skunk ha rociado o ha sido golpeado por un vehículo. A medida que una persona se acerca a la fuente del hedor skunk, el aroma se vuelve más fuerte, porque las «moléculas de hedor» están más concentradas cerca de la fuente.
las moléculas no solo viajan a través del aire sino también a través de otros medios., Cuando una persona pone crema en su café, las moléculas de crema eventualmente rebotan en la taza, moviéndose hacia abajo en el gradiente de concentración hasta que se distribuyen uniformemente. Sin embargo, la mayoría de los bebedores de café no esperan a que esto suceda. Introducen energía adicional agitando el café y acelerando el proceso.
definición del gradiente de concentración Biología
en biología celular, la difusión es una forma principal de transporte de materiales necesarios como aminoácidos dentro de las células., La difusión de disolventes, como el agua, a través de una membrana semipermeable, se clasifica como ósmosis.
el metabolismo y la respiración dependen en parte de la difusión, además de los procesos masivos o activos. Por ejemplo, en los alvéolos de los pulmones de mamíferos, debido a las diferencias en las presiones parciales a través de la membrana alveolar-capilar, el oxígeno se difunde en la sangre y el dióxido de carbono se difunde. Los pulmones contienen una gran superficie para facilitar este proceso de intercambio de gases.
¿qué tiene que ver un gradiente de concentración con una caminata aleatoria?,
¿recuerda el paseo aleatorio sesgado? Bueno, siempre hay una razón para el sesgo. Las bacterias pueden sesgar sus caminatas basadas en el gradiente de concentración de una sustancia química en particular. Así que aunque cada paso está en una dirección aleatoria, la longitud del paso es más larga si la bacteria se está moviendo hacia una concentración más alta que si la bacteria se está moviendo hacia una concentración más baja.
veamos el video de paseo aleatorio sesgado de nuevo, esta vez con el gradiente de concentración en el fondo. Ahora se puede ver la razón de la parcialidad en la caminata!,
¿cómo pueden las bacterias saber si se están moviendo hacia una concentración más alta o más baja?
cuando una bacteria está buscando una señal química en particular, detecta esta sustancia química a medida que se mueve a lo largo de su camino. Si se está moviendo hacia arriba en el gradiente de concentración, comenzará a detectar las moléculas químicas cada vez con más frecuencia. Si se mueve por el gradiente de concentración, comenzará a detectar las moléculas químicas cada vez con menos frecuencia. Esto determina en última instancia la dirección y la fuerza del sesgo en su paseo aleatorio.,
sistema de no equilibrio
debido a que la difusión química es un proceso de transporte neto, el sistema en el que tiene lugar no es un sistema de equilibrio (es decir, no está en reposo todavía). Muchos resultados en la termodinámica clásica no se aplican fácilmente a los sistemas que no están en equilibrio. Sin embargo, a veces ocurren los llamados estados cuasi-estables, donde el proceso de difusión no cambia en el tiempo, donde los resultados clásicos pueden aplicarse localmente. Como su nombre indica, este proceso no es un verdadero equilibrio ya que el sistema aún está evolucionando.,
los sistemas de fluidos sin equilibrio pueden modelarse con éxito con la hidrodinámica fluctuante de Landau-Lifshitz. En este marco teórico, la difusión se debe a fluctuaciones cuyas dimensiones van desde la escala molecular hasta la escala macroscópica.
la difusión química aumenta la entropía de un sistema, es decir, la difusión es un proceso espontáneo e irreversible., Las partículas pueden extenderse por difusión, pero no se reordenan espontáneamente (sin cambios en el sistema, asumiendo que no hay creación de nuevos enlaces químicos, y sin fuerzas externas que actúen sobre la partícula).
lea también: calculadora antiderivada – Una breve introducción