Figur 1. Den kanoniske og ikke-kanoniske NF-kB signalvej
Hvad er NF-kB?
NF-kB er et kort navn på Nuclear Factor kappa-light-chain-enhancer af aktiverede B-celler. Det er ikke et enkelt protein, men en lille familie af inducerbare transkriptionsfaktorer, der spiller en vigtig rolle i næsten alle pattedyrceller. Det kontrollerer DNA-transkription, cytokinproduktion, celleoverlevelse og andre vigtige cellehændelser, spiller især en nøglerolle i reguleringen af immunresponset mod infektion.
NF-kB molekylær er normalt dimerer., En typisk struktur af NF-kB er P50-P65 dimer (NF-KB1/RelA). Dimerdannelsen er nødvendig for DNA-binding, to NF-kB-monomerer binder til DNA som en dimer. De N-terminale regioner af dimer er ansvarlige for specifik DNA-kontakt. De C-terminale regioner er normalt stærkt konserverede, de er ansvarlige for dimerisering og ikke-specifik DNA-fosfatkontakt. Hele NF-kB molekylær er ligesom en tang skruestik på DNA-kæden og fungerer som en transskriptionsfaktor (figur 2).
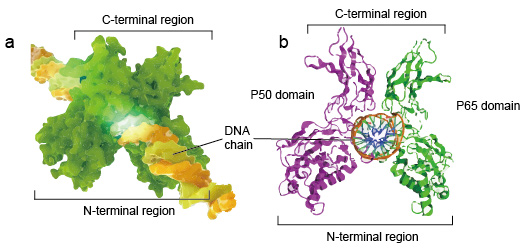
Figur 2. Strukturen af NF-kB protein dimer binding med DNA kæde.,
NF-kB familie
fordi NF-kB familiemedlemmer deler strukturel homologi med retroviral oncoprotein v-Rel. så de kaldte også NF-kB/Rel proteiner. NF-kB transskription faktor familie i pattedyr, der består af 5 proteiner: p65/RelA, RelB, c-Rel, p105/p50 (NF-kB1), og p100/p52 (NF-kB2). Disse 5 proteiner forbinder hinanden og danner forskellige transkriptionelt aktive homo/heterodimere komplekser (figur 3). De deler alle et fælles bevaret rel homology domæne (RHD) af 300 aa længde., Disse RHD-domæner har flere funktioner såsom dimerisering, DNA-binding, interaktion med IkBs og nuklear translokation. Selvom NF-kB-proteinfamiliemedlemmerne kan danne op til 15 forskellige dimerer, men mange af dem har endnu ikke demonstreret. Den mest rigelige form for NF-kB dimer er P50 / P65 heterodimer, som har været fond i næsten alle celletyper. Da kun P65/ Rel, RelB og c-Rel har Carbo .y-terminale transaktionsdomæner (TAD), kan NF-kB-familien af proteiner yderligere opdeles i to grupper., p50 og P52 genereres ved bearbejdning af henholdsvis prækursormolekylerne P105 og P100. Derfor er ikke alle kombinationer af Rel dimerer transkriptionelt aktive.
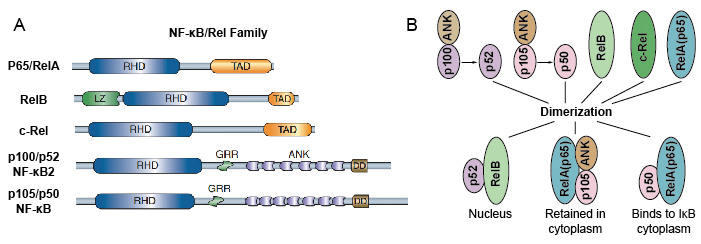
Figur 3. De 5 protein og deres homo / heterodimere komplekser af NF-kB familie.
NF-kB signalvej
NF-kB protein lysdæmpere som nuklear transkriptionsfaktor skal de migrere til kernen kombineret med DNA for at have funktion. I de fleste typer af de normale celler under hviletilstand var NF-KB inaktiv og fastholdt i cytoplasmaet., De binder til en specifik inhibitor kaldet IK-B protein, som kunne binde til Rel homology domain (RHD) af NF-kB og forstyrre dets nukleare lokaliseringssekvens (NLS) funktion. Disse inhibitorproteiner, som omfatter IkBa, IkBb og IkBg, indeholder 6-7 ankyrin-gentagelser, der medierer binding til RHD. Disse gentagelser er også til stede i de C-terminale halvdele af NF-kB2/P100 og NF-KB1/P105 precursorer, som også fungerer som IkBs og bevarer deres partnere, Rel-proteinerne, i cytoplasmaet., For at aktivere NF-kB-molekylæren skal cellerne først adskille NF-kB-proteinet fra deres hæmmere. Der er to vigtige signalveje, der fører til IK-B-proteininhibitoren dissociation fra NF-kB dimmer og lad translokationen af NF-kB dimerer fra cytoplasmaet ind i kernen.
1., Canonical/Klassisk Cascade
Canonical eller klassisk cascade signaler startende fra den celle overflade receptor af pro-inflammatoriske cytokiner, og pathogen-associated molecular patterns (PAMPs), såsom tumor nekrose faktor receptor (TNFR), toll-like receptor (TLR) og T/B-celle receptoren. Disse receptorer, der binder med deres ligandmolekyler og overfører signalet over cellemembranen, forårsager aktiveringen af IkB-kinase (IKK) – komplekset. Den mest almindelige form for dette kompleks består heterodimer af IKKa og ikk and katalytiske underenheder og en IKKy regulatorisk underenhed., IKKy-enheden kaldes også NEMO for NF-kB essential modulator. Den aktiverede IKK komplekse, overvejende handler gennem IKKß i en IKKy-afhængig måde, katalyserer fosforylering af IkBs (på websteder, der svarer til Ser32 og Ser36 af IkBa), polyubiquitination (på websteder, der svarer til Lys21 og Lys22 af IkBa) og efterfølgende nedbrydning af 26S proteasome. De frigivne NF-kB dimerer (oftest p50–RelA dimer), translokerer til kernen, binder DNA og aktiverer do .n-stream gentranskriptionen.
2., Ikke-kanoniske/Alternativ vej Cascade
en Anden NF-kB aktivering af vejen hedder ikke-kanoniske eller alternative vej. Denne vej er uafhængig af ikk and og IKKy, men afhængig af IKKa lysdæmper i stedet. Signaloverførslen til cytoplasmaet gennem LT-or-eller BAFF-receptoren. Phosphonat et NIK-protein, NIK-protein derefter phosphonerer IKKa-homodimmerne. Målet for IKKa-homodimere i denne vej er NF-KB2 / P100, som phosphoryleres på to C-terminaler., Phosphorylering af disse steder er afgørende for P100-forarbejdning til p52, som også er afhængig af polyubi .uitination og proteasomal nedbrydning. I stedet for at føre til fuldstændig P100-nedbrydning, som det ses med IkBs, resulterer den phosphoryleringsafhængige UBI .uitinering af p100 imidlertid kun i nedbrydning af dens hæmmende C-terminale halvdele. Når den C-terminale halvdel er nedbrudt, frigives den N-terminale del af NF-kB (P52-polypeptidet, der indeholder RHD)., Da RHD af p100 oftest er forbundet med RelB, resulterer aktivering af denne ‘alternative’ vej i nuklear translokation af P52–RelB dimerer. Dimeren binder til sidst til DNA og aktiverer do .n-stream gentranskriptionen.
3. Vejregulering
UBI .uitin er et 76-aminosyreprotein, der er stærkt konserveret og allestedsnærværende udtrykt i alle eukaryoter fra gær til menneske. Den carboxylsyre i den C-terminale glycin af ubiquitin kan være kovalent forbundet til de epsilon amin af lysin på et andet protein gennem en isopeptide bond. Denne proces kaldes”allestedsnærværende”., Desuden, den C-terminale hale af ubiquitin kan være direkte knyttet til den N-terminale methionin af en anden ubiquitin til at danne lineær polyubiquitin kæde. UBI .uitination spiller en væsentlig rolle i reguleringen af NF-kB-veje. I ustimulerede celler binder NF-kB sig til inhiberende proteiner fra kB-familien (IkB) og sekvestreres i cytoplasmaet., Efter stimulering phosphoryleres IkB af IkB-kinase (IKK)-komplekset, phosphoryleres IkB efterfølgende UBI .uitineret og nedbrydes af 26S proteasom, hvilket tillader NF-kB at translokere til kernen, hvor det regulerer ekspressionen af en overflod af gener. Som den regulatoriske underenhed af IKK-komplekset er NEMO blevet foreslået at være nøglefaktoren for transducering af UBI .uitinationssignal til IKK-aktivering. Flere DUBs fungerer som vigtige negative regulatorer af IKK for at tillade en stram kontrol af NF-kB-aktivering., En af de bedst undersøgte DUBs er A20, er Det blevet foreslået, at A20 undertrykke hyperactivation af NFkB af deubiquitinating K63-forbundet polyubiquitin knyttet til RIP1 gennem den N-terminale OTU domænet, samt at fremme K48-forbundet polyubiquitination af RIP1 for proteasomal nedbrydning.
4. Nedstrøms signalering
NF-kB fungerer som en central mediator af immun-og inflammatoriske reaktioner og er involveret i stressresponser og regulering af celleproliferation og apoptose. De respektive NF-kB-målgener gør det muligt for organismen at reagere effektivt på disse miljøændringer., Den klassiske NF-kB-vej aktiveres af en række inflammatoriske signaler, hvilket resulterer i koordinatekspression af flere inflammatoriske og medfødte immungener. De proinflammatoriske cytokiner IL-1b og TNF-a aktiverer NF-kB, og deres ekspression induceres som respons på NF-kB-aktivering, hvilket danner en forstærkende fremføringssløjfe. Den alternative vej for NF-kB resultater i nukleare translokation af p52–RelB dimerer, er strengt afhængig af IKKa homodimers og aktiveres af LTbR, BAFF og CD40L ved NIK., Mange data tyder stærkt på, at den alternative vej spiller en central rolle i ekspressionen af gener involveret i udvikling og vedligeholdelse af sekundære lymfoide organer. Transkriptionsfaktorerne i NF-kB-familien styrer udtrykket af et stort antal målgener som reaktion på ændringer i miljøet og derved hjælper med at orkestrere inflammatoriske og immunresponser.
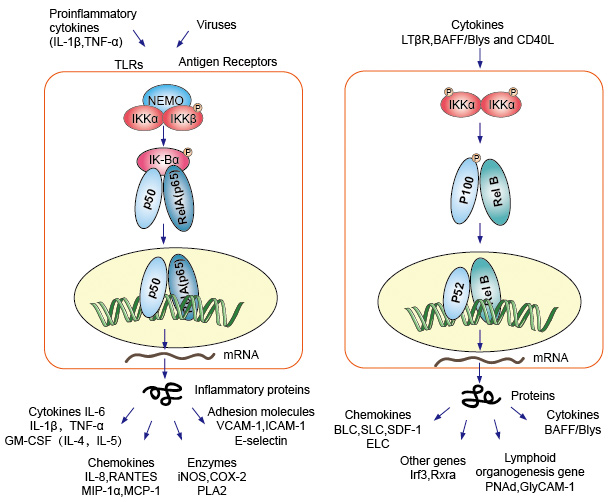
Figur 4. Do .n-stream signalering af NF-kB signalvejen.
5. Forhold til sygdomme.
- det inflammatoriske grundlag for metaboliske sygdomme.,
IKK / NF-kB signalvejen er nøglen til forbindelsen mellem metabolisme, inflammation og insulinvirkning. De fleste af de metaboliske stresssignaler, der resulterer i insulinresistens eller pancreas dysfunction-celledysfunktion, hvad enten det er induceret af intracellulære eller ekstracellulære signaler, konvergerer på den NF-kB-aktiverende kinase IKKb og anden større inflammatorisk kinase, JNK-mitogenaktiveret proteinkinase (MAPK).
- NF-kB og glycolyse.
glykolyse kan generere ATP i større mængder og hurtigere end O .idativ phosphorylering., Glukose er derfor et vigtigt næringsstof for kræft og normale prolifererende celler. NF-kB koordinerer mange af de signaler, der driver celleaktivering og proliferation under immunitet, betændelse og onkogenese.
- NF-kB og O andidativ metabolisme.
NF-kB regulerer energihomeostase og metabolisk tilpasning ved at kontrollere balancen mellem glycolyse og respiration for energiforsyning. Inhibering af NF-kB / RelA på forskellige måder formindskede iltforbruget og forårsagede omprogrammering til aerob glykolyse